题目内容
下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是 (填元素符号,下同).
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式: ,碱性最强的化合物的电子式: .该化合物含有的化学键是
(3)最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠反应的离子方程式: .
| 周期\主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式:
(3)最高价氧化物是两性氧化物的元素是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,①②③④⑤⑥⑦⑧⑨分别是C、N、O、Na、Al、S、Cl、Ar、K元素,
(1)在这些元素中,化学性质最不活泼的是稀有气体元素;
(2)非金属性越强的元素,其最高价氧化物的水化物酸性越强,金属性越强的元素,其最高价氧化物的水化物碱性越强;
(3)最高价氧化物是两性氧化物的元素是Al,氧化铝属于两性氧化物,能和氢氧化钠溶液反应生成偏铝酸钠和水.
(1)在这些元素中,化学性质最不活泼的是稀有气体元素;
(2)非金属性越强的元素,其最高价氧化物的水化物酸性越强,金属性越强的元素,其最高价氧化物的水化物碱性越强;
(3)最高价氧化物是两性氧化物的元素是Al,氧化铝属于两性氧化物,能和氢氧化钠溶液反应生成偏铝酸钠和水.
解答:
解:根据元素在周期表中的位置知,①②③④⑤⑥⑦⑧⑨分别是C、N、O、Na、Al、S、Cl、Ar、K元素,
(1)在这些元素中,化稀有气体元素的原子最外层达到8电子稳定结构,所以既不容易失去电子也不容易得电子,所以化学性质最不活泼的是Ar,故答案为:Ar;
(2)这几种元素中,非金属性最强的是Cl元素,所以其最高价氧化物的水化物酸性最强,化学式为HClO4;金属性最强的元素是K元素,则KOH的碱性最强,电子式为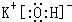 ,KOH中钾离子和氢氧根离子之间存在离子键,O原子和H原子之间存在共价键,所以KOH中存在离子键和共价键,故答案为:HClO4;
,KOH中钾离子和氢氧根离子之间存在离子键,O原子和H原子之间存在共价键,所以KOH中存在离子键和共价键,故答案为:HClO4;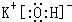 ;离子键和共价键;
;离子键和共价键;
(3)最高价氧化物是两性氧化物的元素是Al,氧化铝属于两性氧化物,能和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al;Al2O3+2OH-=2AlO2-+H2O.
(1)在这些元素中,化稀有气体元素的原子最外层达到8电子稳定结构,所以既不容易失去电子也不容易得电子,所以化学性质最不活泼的是Ar,故答案为:Ar;
(2)这几种元素中,非金属性最强的是Cl元素,所以其最高价氧化物的水化物酸性最强,化学式为HClO4;金属性最强的元素是K元素,则KOH的碱性最强,电子式为
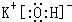 ,KOH中钾离子和氢氧根离子之间存在离子键,O原子和H原子之间存在共价键,所以KOH中存在离子键和共价键,故答案为:HClO4;
,KOH中钾离子和氢氧根离子之间存在离子键,O原子和H原子之间存在共价键,所以KOH中存在离子键和共价键,故答案为:HClO4;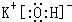 ;离子键和共价键;
;离子键和共价键;(3)最高价氧化物是两性氧化物的元素是Al,氧化铝属于两性氧化物,能和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al;Al2O3+2OH-=2AlO2-+H2O.
点评:本题考查了元素周期表和元素周期律的综合应用,涉及离子方程式的书写、电子式的书写等知识点,这些都是考试热点,知道离子方程式书写规则、电子式书写规则,题目难度不大.

练习册系列答案
相关题目
下列反应中,HCl既表现出酸性又表现出氧化性的是( )
| A、Zn+2HCl=ZnCl2+H2↑ | ||||
B、2HCl
| ||||
C、MnO2+4HCl(浓)
| ||||
| D、HCl+AgNO3=AgCl↓+HNO3 |
如图所示,A、E为石墨电极,B、F为铁片电极.则下列有关推断错误的是( )
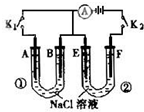

| A、当打开K2,闭合K1时,阳离子向A极移动 |
| B、当打开K1,闭合K2时,电解一段时间在②处可看到沉淀 |
| C、在U形管②中滴入酚酞试液,当打开K1,闭合K2时,E极周围溶液显红色 |
| D、在U形管①中滴入酚酞试液,当打开K2,闭合K1时,B极周围溶液显红色 |