题目内容
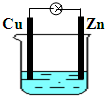
右图为某原电池的装置,下列有关该原电池的说法中正确的是( )
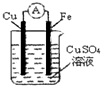
| A.铁棒为正极 |
| B.铜棒上发生还原反应 |
| C.铁棒质量增加 |
| D.电流从铁棒经外电路流向铜棒 |

A.铁比铜活泼,应为原电池的负极,故A错误;
B.铜为正极,正极发生还原反应,故B正确;
C.铁为负极,被氧化,质量减小,故C错误;
D.电流由铜棒经外电路流向铁棒,故D错误.
故选B.
B.铜为正极,正极发生还原反应,故B正确;
C.铁为负极,被氧化,质量减小,故C错误;
D.电流由铜棒经外电路流向铁棒,故D错误.
故选B.

练习册系列答案
相关题目
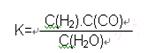
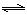 2CO(g),K1
2CO(g),K1 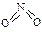 和
和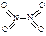 。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为 。
。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为 。 、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。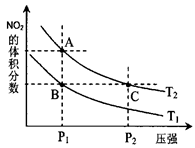
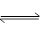 2SO3”为可逆反应,请回答:
2SO3”为可逆反应,请回答: