题目内容
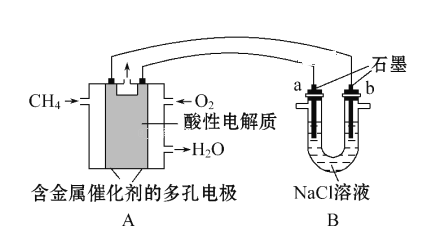
【题目】用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O
C. 阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D. 除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ + 5Cl-+ H2O
【答案】D
【解析】
A、根据电解的原理,铁作阳极时,铁失电子,参与反应,但根据题中信息,铁不参与反应,因此铁作阴极,故A说法正确;B、根据信息,环境是碱性,利用ClO-氧化CN-,因此阳极反应式为Cl-+2OH--2e-=ClO-+H2O,故B说法正确;C、根据电解原理,阴极上是阳离子放电,即2H++2e-=H2↑,故C说法正确;D、CN-被ClO-氧化成两种无毒的气体,即为N2和CO2,环境是碱性,不能生成H+,故D说法错误。

练习册系列答案
相关题目