题目内容
【题目】在3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的分子个数比为
A.2︰1 B.1︰2 C.3︰1 D.1︰3
【答案】B
【解析】
试题分析:在3NO2+H2O=2HNO3+NO中,参加反应的3个NO2中,有2个NO2中N元素的化合价升高到+5价,所以2个NO2做还原剂;1个NO2中N元素的化合价降低,作氧化剂,所以氧化剂与还原剂的分子个数比为1:2,答案选B。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
【题目】除去下列物质中的杂质,所用试剂和方法正确的是( )
选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
A | KCl溶液 | I2 | 蒸馏 |
B | KNO3 | K2SO4 | BaCl2溶液,过滤 |
C | Cu | CuO | 稀硫酸,过滤 |
D | CaCO3 | Ca(OH)2 | 盐酸,过滤 |
A. A B. B C. C D. D
【题目】海洋动物海鞘中含有种类丰富、结构新颖的次生代谢产物,是海洋抗肿瘤活性物质的重要来源之一。一种从海鞘中提取具有抗肿瘤活性的天然产物的流程如下:
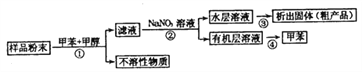
下列关于该流程中各步骤的说法中,错误的是( )
选项 | 步骤 | 采用装置 | 主要仪器 |
A | ① | 过滤装置 | 漏斗 |
B | ② | 分液装置 | 分液漏斗 |
C | ③ | 蒸发装置 | 坩埚 |
D | ④ | 蒸馏装置 | 蒸馏烧瓶 |
A. A B. B C. C D. D