题目内容
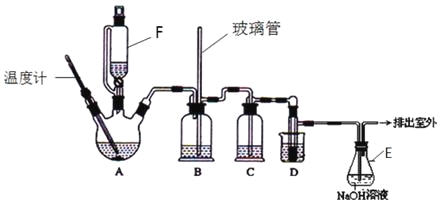
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中A和F中装有乙醇和浓硫酸的混合液,D中的试管里装有液溴.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。(夹持装置已略去)
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g· cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | -1l6 |
填写下列空白:
(1)A中主要发生的是乙醇的脱水反应,即消去反应,请你写出乙醇的这个消去反应的化学方程式: 。
D中发生反应的化学方程式为: 。
(2)安全瓶B可以防止倒吸,并可以检查实验进行时导管是否发生堵塞.请写出发生堵塞时瓶B中的现象 。
(3)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)容器E中NaOH溶液的作用是 。
(5)若产物中有少量副产物乙醚.可用________(填操作名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是_____________。
【答案】(1) CH3CH2OH![]() CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br;
CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br;
(2) b中水面会下降,玻璃管中的水柱会上升,甚至溢出;
(3) C
(4)吸收挥发出来的溴,防止污染环境
(5) 蒸馏
(6)1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞;
【解析】试题分析:(1) 乙醇发生消去反应生成乙烯和水,方程式为:CH3CH2OH![]() CH2=CH2↑+H2O,D中乙烯和溴发生加成反应生成1,2-二溴乙烷,方程式为:CH2=CH2+Br2→CH2BrCH2Br;(2)若装置中出现堵塞,则b中水面会下降,玻璃管中的水柱会上升,甚至溢出;(3)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫 ,二氧化碳、二氧化硫能和氢氧化钠溶液反应,所以在装置C中应加入氢氧化钠溶液,吸收反应中可能生成的酸性气体,所以选C;(4)氢氧化钠能和溴反应生成溴化钠和次溴酸钠和水,所以用氢氧化钠可以吸收挥发出来的溴,防止污染环境。(5)1,2-二溴乙烷沸点132℃,乙醚34.6℃,1,2-二溴乙烷与乙醚的沸点相差较大,两者均为有机物,互溶,用蒸馏的方法将它们分离;(6)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞。
CH2=CH2↑+H2O,D中乙烯和溴发生加成反应生成1,2-二溴乙烷,方程式为:CH2=CH2+Br2→CH2BrCH2Br;(2)若装置中出现堵塞,则b中水面会下降,玻璃管中的水柱会上升,甚至溢出;(3)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫 ,二氧化碳、二氧化硫能和氢氧化钠溶液反应,所以在装置C中应加入氢氧化钠溶液,吸收反应中可能生成的酸性气体,所以选C;(4)氢氧化钠能和溴反应生成溴化钠和次溴酸钠和水,所以用氢氧化钠可以吸收挥发出来的溴,防止污染环境。(5)1,2-二溴乙烷沸点132℃,乙醚34.6℃,1,2-二溴乙烷与乙醚的沸点相差较大,两者均为有机物,互溶,用蒸馏的方法将它们分离;(6)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO![]() ,反应的离子方程式为______________,同时V2O4转化成VO2+。“废渣1”的主要成分是________。
,反应的离子方程式为______________,同时V2O4转化成VO2+。“废渣1”的主要成分是________。
(2)“氧化”中欲使3 mol的VO2+变为VO![]() ,则需要氧化剂KClO3至少为________mol。
,则需要氧化剂KClO3至少为________mol。