题目内容
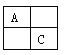
【题目】(14分)A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
(1)D的离子结构示意图为_____________。
(2)B、C、D形成的简单离子半径由大到小的顺序: > > (写离子符号)
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到60 mL 10.0 mol/L乙的浓溶液中,充分反应,共收集到4.48L(标准状况)气体,则该气体的成分是_________,反应中电子转移数为____________。若使上述中反应后剩余的铜片继续溶解,可向其中加入稀硫酸,写出反应的离子方程式: 。
(4)将两份足量的B单质分别加入到等体积等浓度的硫酸和NaOH溶液中,充分反应生成气体的体积比为__________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_____________________________________。
【答案】(共14分)
(1) (2分)
(2分)
(2)S2-> Cl->Al3+ (2分)
(3)NO2 NO (2分 多写少些均不得分 )
0.4 mol(2分) 3Cu+8H++2NO3-=3Cu2++2NO +4H2O(2分)
(4) 2:3(2分) Al3++3[Al(OH)4 ] -="4" Al(OH)3(2分)
【解析】试题分析:A元素最外层与次外层上的电子数之差为3,根据A在元素周期表中的位置,可知A为N元素,则C为S元素,A、B、C、D是原子序数依次增大的短周期主族元素,则D为Cl元素,因为B为地壳中含最最多的金属元素,则B为Al元素。
(1)D为Cl元素,则D离子为Cl,结构示意图为:
(2)B、C、D形成的简单离子分别为Al3+、S2、Cl,根据电子层数越大,离子半径越大;电子排布相同的离子,原子序数越大,离子半径越小,所以B、C、D形成的简单离子半径由大到小的顺序为:S2-> Cl->Al3+
(3)A的最高价氧化物对应的水化物是HNO3,因为Cu过量,随着反应的进行,HNO3的物质的量逐渐减少,浓硝酸变为稀硝酸,所以生成的气体为NO2和NO;HNO3物质的量为0.06L×10.0 molL1=0.6mol,生成的的气体在标准状况下的体积为4.48L,则物质的量为0.2mol,因为Cu过量,HNO3完全反应,起酸性作用的硝酸物质的量为:0.6mol-0.2mol=0.4mol,根据Cu(NO3)2的组成可知反应的Cu物质的量为0.2mol,根据Cu化合价的变化可知电子转移数为0.4 mol;加入稀硫酸后,NO3、H+可以继续与Cu反应,离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO +4H2O。
(4)Al与硫酸反应的化学方程式为:2Al+3H2SO4=2Al2(SO4)3+3H2↑,Al与NaOH溶液反应的化学方程式为:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑因为H2SO4与NaOH物质的量相等,所以生成气体的体积比为:2:3;将反应后所得的溶液混合,Al3+与[Al(OH)4]发生水解反应,会生成白色沉淀Al(OH)3,所以发生反应的离子方程式为: Al3++3[Al(OH)4 ] -="4" Al(OH)3

【题目】下表是元素周期表的前三周期:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0[ | |
一 | A | |||||||
二 | B | C | D | E | F | |||
三[ | G | H | I | J |
回答下列问题:
(1)J元素的元素的名称:___________。
(2)G元素与I 元素形成的化合物的电子式是___________,
A、G、E形成的化合物中含有的化学键类型为_____________________________。
(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是_____________,
属于两性氢氧化物的是_______________(用化合物的化学式表示)。
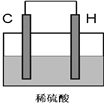
(4)将H单质与C的一种单质(导体)按如下图装置连接,其中C极为_________极(填正或负),并写出该电极反应式为:____________________。