题目内容
【题目】已知:![]()
![]()
![]() (R、R'可表示烃基或官能团)。A可发生如图转化(方框内物质均为有机物,部分无机产物已略去):
(R、R'可表示烃基或官能团)。A可发生如图转化(方框内物质均为有机物,部分无机产物已略去):
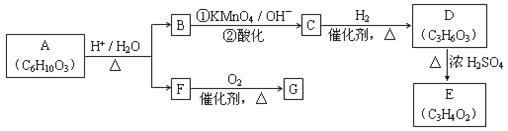
请回答:
(1)F的蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1mol F与足量金属钠作用产生H2 22.4L(标准状况),则F的分子式是_____,名称是__________.
(2)G与F的相对分子质量之差为4,则G具有的性质是______(填字母)
a.可与银氨溶液反应 b.可与乙酸发生酯化反应
c.可与氢气发生加成反应 d.1mol G最多可与2mol新制Cu(OH)2发生反应
(3)D能与NaHCO3溶液发生反应,且两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是______________,该反应类型是_____反应
(4)H与B互为同分异构体,且所含官能团与B相同,则H的结构简式可能是:_________.
(5)A转化为B和F的化学方程式是__________.
(6)A的同分异构体含有两种官能团,该化合物能发生水解,且1mol该化合物能与4mol银氨溶液反应,符合该条件的同分异构体一共有__________种。
【答案】C2H6O2 乙二醇 ac CH3CH(OH)COOH![]() CH2=CHCOOH+H2O 消去 CH2=CHCH2COOH、CH3CH=CHCOOH
CH2=CHCOOH+H2O 消去 CH2=CHCH2COOH、CH3CH=CHCOOH ![]() +H2O
+H2O![]()
![]() +HOCH2CH2OH 12
+HOCH2CH2OH 12
【解析】
F的蒸气密度是相同条件下H2密度的31倍,则其相对分子质量为62,1mol F与足量金属钠作用产生H222.4L(标准状况),即1molH2,说明F中很有2个-OH,应为乙二醇,即C2H6O2,被催化氧化生成醛,根据R-CH2OH→RCHO可知,二者相对分子质量相差2,G与F的相对分子质量之差为4,则G应为OHC-CHO,为乙二醛;A生成B和F的反应应为酯的水解,则B的分子式应为C4H6O2,结合题给信息可知应为![]() ,A为
,A为![]() ,C为
,C为![]() ,与氢气发生加成反应生成D,D应为CH3CH(OH)COOH,CH3CH(OH)COOH在浓硫酸作用下发生消去反应生成E,则E为CH2=CHCOOH,结合有机物的结构和性质解答该题。
,与氢气发生加成反应生成D,D应为CH3CH(OH)COOH,CH3CH(OH)COOH在浓硫酸作用下发生消去反应生成E,则E为CH2=CHCOOH,结合有机物的结构和性质解答该题。
(1)F的蒸气密度是相同条件下H2密度的31倍,则其相对分子质量为62,1mol F与足量金属钠作用产生H2 22.4L(标准状况),即1molH2,说明F中很有2个﹣OH,应为乙二醇,即C2H6O2;
故答案为:C2H6O2;乙二醇;
(2)G应为OHC﹣CHO,为乙二醛,含有﹣CHO,可发生氧化和加成反应,不能发生酯化反应,因含有2个﹣CHO,则1molG最多可与4mol新制Cu(OH)2发生反应;
故答案为:ac;
(3)D应为CH3CH(OH)COOH,CH3CH(OH)COOH在浓硫酸作用下发生消去反应生成E,则E为CH2=CHCOOH,反应的方程式为CH3CH(OH)COOH![]() CH2=CHCOOH+H2O;
CH2=CHCOOH+H2O;
(4)B为![]() ,H与B互为同分异构体,且所含官能团与B相同,可为CH2=CHCH2COOH、CH3CH=CHCOOH;
,H与B互为同分异构体,且所含官能团与B相同,可为CH2=CHCH2COOH、CH3CH=CHCOOH;
(5)A为![]() ,可水解生成
,可水解生成![]() 和乙二醇,反应的方程式为
和乙二醇,反应的方程式为![]() +H2O
+H2O![]()
![]() +HOCH2CH2OH;
+HOCH2CH2OH;
(6)A的同分异构体含有两种官能团,该化合物能发生水解,且1mol该化合物能与4mol银氨溶液反应,含有2个醛基,所以分子中不含醚键,只能为一个醛基一个甲酸酯基,共有12种结构。

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为___,电池反应的离子方程式为___。
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn___g。(已经F=96500C/mol)
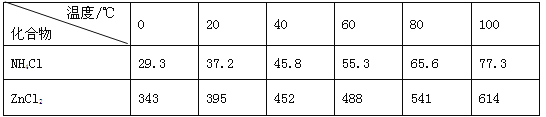
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过___分离回收;滤渣的主要成分是MnO2、___和_______,欲从中得到较纯的MnO2,最简便的方法是___,其原理是___。