题目内容
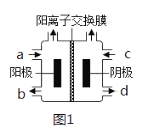
【题目】某化学兴趣小组的同学设计了如图所示的装置,完成下列问题:
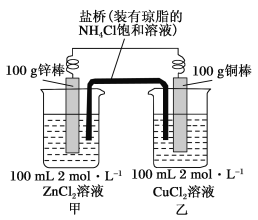
(1)反应过程中,_____棒质量减少,当一电极质量增加2 g,另一电极减轻的质量_____(填“大于”、“小于”或“等于”)2g,正极的电极反应为_______。
(2)盐桥的作用是向甲、乙两烧杯中提供NH![]() 和Cl-,使两烧杯溶液中保持电荷守恒。
和Cl-,使两烧杯溶液中保持电荷守恒。
①反应过程中Cl-将进入______(填“甲”或“乙”)烧杯。
②当外电路中转移0.2 mol电子时,乙烧杯中浓度最大的阳离子是______。
【答案】锌 大于 Cu2++2e-=Cu 甲 NH4+
【解析】
锌比铜活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为Cu2++2e-=Cu,结合电极方程式解答该题;
(1) 锌比铜活泼,锌为负极,铜为正极,铜电极析出铜;
(2)盐桥的作用是向甲、乙两烧杯中提供NH![]() 和Cl-,使两烧杯溶液中保持电荷守恒。
和Cl-,使两烧杯溶液中保持电荷守恒。
①原电池中阴离子移向负极,阳离子移向正极;
②乙烧杯中铜离子析出,电荷守恒计算铵根离子浓度。
锌比铜活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为Cu2++2e-=Cu;
(1)反应过程中,锌棒是负极,发生氧化反应,质量减小,而铜棒是正极,发生还原反应,电极反应式为Cu2++2e-=Cu,则正极上质量增重,当正极质量增加2g时,转移电子的物质的量为![]() ×2mol=
×2mol=![]() mol,此时负极质量减少
mol,此时负极质量减少![]() mol×65g/mol×
mol×65g/mol×![]() >2g;
>2g;
(2) ①反应过程中,盐桥中的Cl-移向负极锌,Cl-进入甲杯;
②当外电路中转移0.2mol电子时,Cu2++2e-=Cu,铜离子减少0.1mol,电荷减少0.2mol,溶液中进入NH4+0.2mol,乙烧杯中浓度最大的阳离子是NH4+,其浓度=![]() =2mol/L。
=2mol/L。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案