题目内容
 (2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)
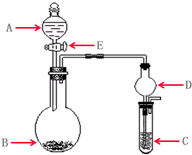
(2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)(1)若A中为30%的H2O2溶液,B中固体为MnO2,C中盛有FeCl2和KSCN的混合液,旋开E后,C中的现象是
有气泡逸出,试管中溶液变为红色
有气泡逸出,试管中溶液变为红色
,C中发生氧化还原反应的离子方程式是4Fe2++O2+4H+=4Fe3++2H2O
4Fe2++O2+4H+=4Fe3++2H2O
.(2)若A中为浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,旋开E后,B中出现黄绿色气体.已知1mol KMnO4发生反应时转移5mol电子,且生成的气体为单质.B中发生反应的化学方程式是
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
,C中的现象是溶液变蓝
溶液变蓝
;继续反应一段时间后,发现C中溶液的颜色褪去,这是因为在溶液中碘单质被过量的氯气氧化(生成IO3-),所以蓝色褪去
碘单质被过量的氯气氧化(生成IO3-),所以蓝色褪去
.有学生认为,此实验装置不符合环保要求,请你提出改进意见在C后增加一个盛有足量NaOH溶液的尾气吸收装置
在C后增加一个盛有足量NaOH溶液的尾气吸收装置
.(3)若B中是生石灰,将A中液体逐滴加入B内,实验中观察到C的溶液中先出现沉淀,然后沉淀逐渐溶解,当溶液恰好澄清时,关闭E,将C装置放入盛有沸水的烧杯中,静置片刻,观察到试管内壁出现光亮的银镜.回答下列问题:
①A中液体的名称是
浓氨水
浓氨水
,C中是葡萄糖与AgNO3
AgNO3
(写化学式)的混合液.②仪器D在此实验中的作用是
防止倒吸
防止倒吸
.分析:(1)根据H2O2溶液在MnO2 作催化剂的条件下分解制氧气,氧气能氧化Fe2+生成Fe3+,Fe3+遇KSCN的溶液变红;
(2)根据浓盐酸能被KMnO4氧化生成氯气,氯气能氧化I-生成I2,氯气过量,碘单质被过量的氯气氧化生成IO3-,过量的氯气会污染环境;
(3)根据银镜反应来分析;
(2)根据浓盐酸能被KMnO4氧化生成氯气,氯气能氧化I-生成I2,氯气过量,碘单质被过量的氯气氧化生成IO3-,过量的氯气会污染环境;
(3)根据银镜反应来分析;
解答:解:(1)因H2O2溶液在MnO2 作催化剂的条件下分解制氧气,有气泡逸出,氧气能氧化Fe2+生成Fe3+,Fe3+遇KSCN的溶液变红,故答案为:有气泡逸出,试管中溶液变为红色;4Fe2++O2+4H+=4Fe3++2H2O
(2)浓盐酸能被KMnO4氧化生成氯气:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,氯气能氧化I-:Cl2+2KI=I2+2KCl,I2遇淀粉变蓝;过量的氯气能继续氧化碘单质生成IO3-,所以蓝色褪去;过量的氯气不吸收直接排空,会污染空气,所以在C后增加一个盛有足量NaOH溶液的尾气吸收装置,
故答案为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;溶液变蓝; 碘单质被过量的氯气氧化(生成IO3-),所以蓝色褪去; 在C后增加一个盛有足量NaOH溶液的尾气吸收装置.
(3)因将A中液体逐滴加入B内,实验中观察到C的溶液中先出现沉淀,然后沉淀逐渐溶解,当溶液恰好澄清时,这是银
银氨溶液的配制,故A中液体为浓氨水,C中是葡萄糖与AgNO3的混合物,因氨气极易溶于水,吸收时要防倒吸,故答案:①浓氨水;AgNO3;②防止倒吸.
(2)浓盐酸能被KMnO4氧化生成氯气:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,氯气能氧化I-:Cl2+2KI=I2+2KCl,I2遇淀粉变蓝;过量的氯气能继续氧化碘单质生成IO3-,所以蓝色褪去;过量的氯气不吸收直接排空,会污染空气,所以在C后增加一个盛有足量NaOH溶液的尾气吸收装置,
故答案为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;溶液变蓝; 碘单质被过量的氯气氧化(生成IO3-),所以蓝色褪去; 在C后增加一个盛有足量NaOH溶液的尾气吸收装置.
(3)因将A中液体逐滴加入B内,实验中观察到C的溶液中先出现沉淀,然后沉淀逐渐溶解,当溶液恰好澄清时,这是银
银氨溶液的配制,故A中液体为浓氨水,C中是葡萄糖与AgNO3的混合物,因氨气极易溶于水,吸收时要防倒吸,故答案:①浓氨水;AgNO3;②防止倒吸.
点评:本题主要考查了气体的制备与性质,根据物质的性质得出实验现象,培养了学生分析问题的能力.

练习册系列答案
相关题目
 (2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
(2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应: p C(g)+q D(g)达到平衡后,测得B的浓度为0.5
p C(g)+q D(g)达到平衡后,测得B的浓度为0.5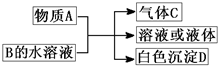 (2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.
(2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.