题目内容
(2011?崇文区模拟)下列说法正确的是( )
分析:A、根据外界条件对化学平衡的影响分析,升高温度平衡向吸热方向移动,增大压强平衡向气体体积减小的方向移动.
B、吸收塔中吸收三氧化硫气体的吸收液的选择及原因;
C、铜棒吸收热量影响测定结果.
D、两次称量的差不超过0.1 g为止.
B、吸收塔中吸收三氧化硫气体的吸收液的选择及原因;
C、铜棒吸收热量影响测定结果.
D、两次称量的差不超过0.1 g为止.
解答:解:A、合成氨反应是一个反应前后气体体积减小的放热反应,升高温度平衡向逆反应方向反应,降低氨气的产率,增大压强平衡向正反应方向移动,提高氨气的产率,故A错误.
B、吸收塔中SO3如果用稀硫酸吸收,发生反应:SO3+H2O═H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,最终得到“发烟”硫酸,故B错误.
C、铜棒吸收热量导致溶液的温度偏小,导致测定结果偏小,故C错误.
D、实验中的加热、冷却、称量的操作步骤要重复进行,直至连续两次称量的差不超过0.1g为止,一般情况下,结晶水含量测定时称量次数不得少于四次,故D正确;
故选D.
B、吸收塔中SO3如果用稀硫酸吸收,发生反应:SO3+H2O═H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,最终得到“发烟”硫酸,故B错误.
C、铜棒吸收热量导致溶液的温度偏小,导致测定结果偏小,故C错误.
D、实验中的加热、冷却、称量的操作步骤要重复进行,直至连续两次称量的差不超过0.1g为止,一般情况下,结晶水含量测定时称量次数不得少于四次,故D正确;
故选D.
点评:本题考查了实验的有关问题,难度不大,会运用化学平衡移动原理分析合成氨条件的选择.

练习册系列答案
相关题目
 (2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
(2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应: p C(g)+q D(g)达到平衡后,测得B的浓度为0.5
p C(g)+q D(g)达到平衡后,测得B的浓度为0.5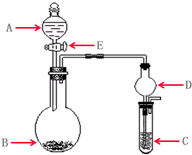 (2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)
(2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)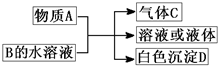 (2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.
(2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.