题目内容
【题目】按下列要求回答:
(1)已知:CH2=CH2+KMnO4+H2SO4→CO2+K2SO4+MnSO4+H2O(未配平)理论上,480mL0.1000molL﹣1酸性KMnO4溶液可氧化乙烯mL(标准状况).
(2)实验室里欲用KMnO4固体来配制480mL 0.1000molL﹣1的酸性KMnO4溶液. ①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、
②下列操作会导致酸性KMnO4溶液浓度偏高的是(填序号).
a.加水定容时俯视刻度线
b.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制
c.容量瓶底部有少量蒸馏水
(3)如图所示装置的气密性检查中,一定漏气的是(填序号). 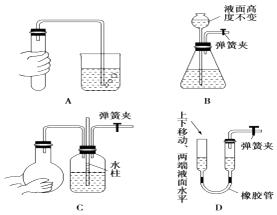
(4)W、X、Y和Z都是周期表中前20号元素,已知: (A) W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
(B) Y和Z属同族元素,它们能形成两种常见化合物;
(C) X和Z属同一周期元素,它们能形成两种气态化合物;
(D) X和Y不在同一周期,它们能形成组成为XY2的非极性分子.
请回答:
①W元素是;Z元素是 .
②化合物WY的电子式为 .
③Y和Z形成的两种常见化合物的分子式是和 .
④写出X和Z形成的一种气态化合物跟WZ反应的化学方程式 .
【答案】
(1)480
(2)胶头滴管、500mL容量瓶;a
(3)D
(4)钙;氧;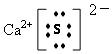 ;SO2;SO3;CO2+CaO=CaCO3
;SO2;SO3;CO2+CaO=CaCO3
【解析】解:(1)乙烯中C元素化合价为﹣2价,被氧化生成二氧化碳,元素化合价升高6价,Mn元素化合价由+7价降低到+2价,n(KMnO4)=0.48L×0.1mol/L=0.048mol, 得到电子的物质的量为0.048mol×5=0.24mol,则n(CH2=CH2)= ![]() =0.02mol,V=0.02mol×22.4L=0.48L=480mL,
=0.02mol,V=0.02mol×22.4L=0.48L=480mL,
所以答案是:480;(2)应配制500mL,需要称量、溶解、移液、定容等操作,需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管以及500mL容量瓶,
a.加水定容时俯视刻度线,导致体积偏小,则浓度偏大,故正确;
b.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制,导致浓度偏小,故错误;
c.容量瓶底部有少量蒸馏水,对实验没有影响,故错误.
所以答案是:胶头滴管、500mL容量瓶;a;(3)A.用手握住试管,试管内气体受热膨胀,在烧杯内有气泡产生,说明装置气密性良好,故A不漏气;
B.用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好,故B不漏气;
C.用弹簧夹夹住右边导管,双手捂住烧瓶,烧瓶内气体受热膨胀,使集气瓶中气体压强增大,在玻璃管中形成一段水柱,说明装置气密性良好,故C不漏气;
D.用弹簧夹夹住右边导管,上下移动,若装置不漏气,两边液面应形成一定的高度差,而图示两端液面相平,说明装置漏气;
所以答案是:D;(4)①由以上分析可知W元素是钙;Z元素是氧,所以答案是:钙;氧;②化合物WY为CaS,为离子化合物,电子式为  ,所以答案是:
,所以答案是:  ;③Y和Z形成的两种常见化合物的分子式是SO2、SO3 , 所以答案是:SO2;SO3;④写出X和Z形成的一种气态化合物跟WZ反应的化学方程式为CO2+CaO=CaCO3 , 所以答案是:CO2+CaO=CaCO3 .
;③Y和Z形成的两种常见化合物的分子式是SO2、SO3 , 所以答案是:SO2;SO3;④写出X和Z形成的一种气态化合物跟WZ反应的化学方程式为CO2+CaO=CaCO3 , 所以答案是:CO2+CaO=CaCO3 .
【考点精析】解答此题的关键在于理解配制一定物质的量浓度的溶液的相关知识,掌握配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线.

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案【题目】已知反应H2(g)+Br2(l)=2HBr(g)在25 ℃、101 kPa下进行,放出热量为72 kJ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
H2(g) | Br2(g) | HBr(g) | |
1 mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为( )。
A.404B.260C.230D.200