题目内容
20.(1)烷烃的通式是:CnH2n+2.烷烃分子中的碳原子数目每增加一个,其相对分子质量增加14.(2)由甲烷制取一氯甲烷的化学方程式CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl.该反应属于取代反应.
(3)①用系统命名法给
 命名:2,2,3,4-四甲基戊烷.
命名:2,2,3,4-四甲基戊烷.②写出2,2-二甲基-3-乙基戊烷的结构简式:CH3C(CH3)(CH3)CH(C2H5)CH2CH3.
分析 (1)烷烃的通式为CnH2n+2,烷烃分子的同系物之间相差1个CH2时,相对分子质量增加14;
(2)甲烷在光照条件下与氯气发生取代反应生成一氯甲烷;
(3)① ,该有机物为烷烃,主链最长碳链含有5个C,编号从右到左,2号C有2个甲基,在3、4号C各含有1个甲基;
,该有机物为烷烃,主链最长碳链含有5个C,编号从右到左,2号C有2个甲基,在3、4号C各含有1个甲基;
②2,2-二甲基-3-乙基戊烷的结构简式为:CH3C(CH3)(CH3)CH(C2H5)CH2CH3.
解答 解:(1)烷烃的通式为CnH2n+2,烷烃分子的同系物之间相差1个CH2或多个CH2原子团,烷烃分子中的碳原子数目每增加一个,相差CH2,其相对分子质量增加14;故答案为:CnH2n+2;14;
(2)甲烷在光照条件下与氯气发生取代反应生成一氯甲烷,方程式为CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl;
故答案为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl;取代反应;
(3)① ,该有机物为烷烃,主链最长碳链含有5个C,主链为戊烷,编号从右到左,2号C有2个甲基,在3、4号C各含有1个甲基,该有机物命名为:2,2,3,4-四甲基戊烷;
,该有机物为烷烃,主链最长碳链含有5个C,主链为戊烷,编号从右到左,2号C有2个甲基,在3、4号C各含有1个甲基,该有机物命名为:2,2,3,4-四甲基戊烷;
故答案为:2,2,3,4-四甲基戊烷;
②2,2-二甲基-3-乙基戊烷的结构简式为:CH3C(CH3)(CH3)CH(C2H5)CH2CH3,
故答案为:CH3C(CH3)(CH3)CH(C2H5)CH2CH3.
点评 本题主要考查了有机物结构简式的书写、命名及甲烷的取代反应,难度不大.要注意掌握有机物的结构特点是解题的关键.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
10. 甲烷分子中的四个氢原子都可以被取代.甲烷分子的四个氢原子都被乙烯基(CH2═CH-)取代得到的产物的结构如图所示.下列对所得分子的描述中不正确的是( )
甲烷分子中的四个氢原子都可以被取代.甲烷分子的四个氢原子都被乙烯基(CH2═CH-)取代得到的产物的结构如图所示.下列对所得分子的描述中不正确的是( )
 甲烷分子中的四个氢原子都可以被取代.甲烷分子的四个氢原子都被乙烯基(CH2═CH-)取代得到的产物的结构如图所示.下列对所得分子的描述中不正确的是( )
甲烷分子中的四个氢原子都可以被取代.甲烷分子的四个氢原子都被乙烯基(CH2═CH-)取代得到的产物的结构如图所示.下列对所得分子的描述中不正确的是( )| A. | 分子式为:C9H12 | |
| B. | 1mol此分子在一定条件下最多能与4mol H2发生加成反应 | |
| C. | 所有碳原子都在同一平面上 | |
| D. | 此物质属于烯烃类物质 |
15.下列表示物质结构的化学用语或模型图正确的是( )
| A. | 14C的原子结构示意图: | B. | 二氧化碳的电子式: | ||
| C. | H2O2的电子式: | D. | C3H8的结构式:CH3-CH2-CH3 |
5. 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
①向溶液中加入1~2滴指示剂.
②取20.00mL标准溶液放入锥形瓶中.
③用氢氧化钠溶液滴定至终点.
④重复以上操作.
⑤配制250mL盐酸标准溶液.
⑥根据实验数据计算氢氧化钠的物质的量浓度.
(1)以上各步中,正确的操作顺序是⑤②①③④⑥(填序号),上述②中使用的仪器除锥形瓶外,还需要酸式滴定管,使用酚酞作指示剂.
(2)滴定并记录V(NaOH)的初、终读数.数据记录如下表:
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积为
V(NaOH)=$\frac{19.98+20.00+20.80+20.02}{4}$mL=20.02mL
他的计算合理吗?不合理.理由是第3组数据明显偏大,不应采用.
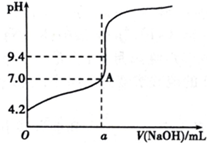
通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如下图所示,则a< 20.02(填“>”“<”或“=”).
 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:①向溶液中加入1~2滴指示剂.
②取20.00mL标准溶液放入锥形瓶中.
③用氢氧化钠溶液滴定至终点.
④重复以上操作.
⑤配制250mL盐酸标准溶液.
⑥根据实验数据计算氢氧化钠的物质的量浓度.
(1)以上各步中,正确的操作顺序是⑤②①③④⑥(填序号),上述②中使用的仪器除锥形瓶外,还需要酸式滴定管,使用酚酞作指示剂.
(2)滴定并记录V(NaOH)的初、终读数.数据记录如下表:
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(标准溶液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
V(NaOH)=$\frac{19.98+20.00+20.80+20.02}{4}$mL=20.02mL
他的计算合理吗?不合理.理由是第3组数据明显偏大,不应采用.
通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如下图所示,则a< 20.02(填“>”“<”或“=”).
12.已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是( )
| A. | A、B、D不可能在同周期 | B. | C和D的单质可能化合为离子化合物 | ||
| C. | A、D可能在同一主族 | D. | D一定在第二周期 |
4.某科研小组设计出利用工业废酸(稀H2SO4)来浸取某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如图所示.

已知:各离子开始沉淀及完全沉淀时的pH如表所示.
请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是适当升高温度(或增大酸浓度、将氧化铜锌矿粉碎等).(任写一点即可)
(2)物质A最好使用下列物质中的B.
A.KMnO4B.H2O2C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2~6.2范围之间.
(4)物质B可直接用作氮肥,则B的化学式是(NH4)2SO4.
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能处理剂--K2FeO4,写出该反应的离子方程式2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.

已知:各离子开始沉淀及完全沉淀时的pH如表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是适当升高温度(或增大酸浓度、将氧化铜锌矿粉碎等).(任写一点即可)
(2)物质A最好使用下列物质中的B.
A.KMnO4B.H2O2C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2~6.2范围之间.
(4)物质B可直接用作氮肥,则B的化学式是(NH4)2SO4.
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能处理剂--K2FeO4,写出该反应的离子方程式2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.
 和
和 ⑤H2O和H2O2
⑤H2O和H2O2 .
. 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.