题目内容
某化学课外活动小组欲制取纯Na2CO3溶液并讨论实验过程中的相关问题。可供选择的试剂有:A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备实验方案的反应流程分别如下:
甲:NaOH溶液![]() Na2CO3溶液
Na2CO3溶液

请完成下列问题:
(1)请指出甲、乙两方案的主要缺点:
甲方案_____________________________________________________________;
乙方案_____________________________________________________________。
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键有_____________________________。
(3)假设反应③所得的NaHCO3溶液中含有Na2CO3,现要利用A—D四种试剂证明Na2CO3的存在,你所选择的试剂有___________(填试剂代号)。
(4)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3。乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学能否达到实验目的?___________(填“能”或“不能”)若能,请说明其计算所需的数据;若不能,请简要说明理由:___________________________。
(1)甲方案CO2的通入量不易控制
乙方案过程烦琐,操作复杂
(2)a.反应③应充分进行
b.反应③与④所用NaOH溶液的体积应相等
(3)A和B
(4)能 固体样品的质量和沉淀总质量
解析:(1)甲方案CO2的通入量不易控制,若CO2不足,Na2CO3
中混有NaOH,若CO2过量,Na2CO3中混有NaHCO3;乙方案过程烦琐,操作复杂。
(2)丙方案制取纯净Na2CO3的关键有两点:①反应③充分进行,NaOH全部转化为NaHCO3,②反应③和④所用NaOH溶液的体积相等。
(3)证明Na2CO3的存在可用大理石与盐酸反应生成可溶性的CaCl2证明。
(4)乙同学能达到实验目的,因为只要准确称量固体样品质量,最终Na2CO3、NaHCO3与澄清石灰水作用均生成CaCO3,只要称量出沉淀的总质量,列方程组计算即可得出实验结果。

物质名称 | 溶解度/g |
NaOH | 110 |
Na2CO3 | 30 |
NaHCO3 | 9 |
(1)用化学方程式表示其制备过程;
(2)若耗用100 g水需NaOH物质的量为____________ mol;
(3)简述实验操作过程;
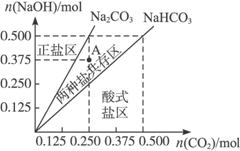
(4)上述上图为该实验过程中的图象,请在图中标出A点,即当n(CO2)∶n(NaOH)=2∶3,且n(CO2)=0.250 mol 时的位置,并由此判断此时所得盐的组成,计算其物质的量。
 请回答下列问题:
请回答下列问题:
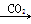 Na2CO3溶液
Na2CO3溶液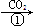 NaHCO3溶液
NaHCO3溶液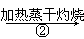 Na2CO3固体
Na2CO3固体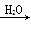 Na2CO3溶液
Na2CO3溶液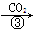 NaHCO3溶液
NaHCO3溶液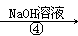 Na2CO3溶液
Na2CO3溶液