题目内容
【题目】在相同温度和压强下,对反应CO2(g)+H2(g)![]() CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入体积不变的容器内各组分的物质的量见下表:
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入体积不变的容器内各组分的物质的量见下表:
CO2 | H2 | CO | H2O | |
甲 | 2a mol | 2a mol | 0 | 0 |
乙 | 2a mol | a mol | 0 | 0 |
丙 | 0 | 0 | 2a mol | 2a mol |
丁 | amol | 0 | a mol | a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A. 乙>丁>甲>丙 B. 乙=丁<丙=甲
C. 丁>乙>丙=甲 D. 丁>丙>乙>甲
【答案】B
【解析】四个容器中若都换算成反应物,则CO2和H2的物质的量(mol)分别为甲:2a、2a;乙:2a、a;丙:2a、2a;丁:2a、a。所以甲=丙,乙=丁。甲容器相当于在乙平衡的基础上又加入了amol的CO2,因此可提高氢气的转化率,生成物CO的物质的量就多。故答案是B。

【题目】据报道:研究人员破解了北京及华北地区雾霾主要成分硫酸盐的形成之谜,发现在大气细颗粒物吸附的水分中NO2与SO2的化学反应是当前雾霾期间硫酸盐的主要生成路径。某实验小组对NO2和SO2的反应进行探究。
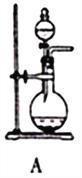

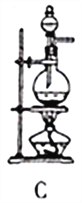
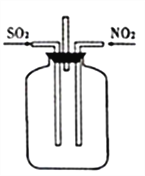
图Ⅰ 图Ⅱ
(1)SO2的发生装置可以选择图Ⅰ中的_______(填字母),反应的化学方程式为___________________。
(2)按图Ⅱ所示进行实验。
①实验时往集气瓶中通入等体积的SO2和NO2,观察到集气瓶中有白烟产生,通入的NO2气体颜色变浅,该反应的化学方程式为______________________。如果集气瓶中有少量水,则可能观察不到白烟,其原因是____________。
②请指出图Ⅱ装置设计的不合理之处___________。
(3)硫酸铵是我国pm2.5雾霾的主要成分,收集一定量的雾霾固体进行验证:
操作步骤 | 实验现象 | 结论 |
取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份。 | ||
一份___________。 | 有白色沉淀生成。 | 证明雾霾固体中含有SO42- |
另一份___________。 | ___________。 | 证明雾霾固体中含有NH4+。综合上面实验,说明雾霾固体颗粒中含有(NH4)2SO4。 |
【题目】如表所示,提纯下列物质(括号内为杂质),所用除杂试剂和分离方法都正确的是
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | 苯中的少量苯酚 | NaOH溶液 | 分液 |
B | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
C | 福尔马林(甲酸) | NaOH溶液 | 分液 |
D | 乙酸乙酯(乙酸) | 饱和的碳酸钠溶液 | 过滤 |
A. A B. B C. C D. D
