题目内容
12.下列化学用语正确的是( )| A. | 聚丙烯的结构简式: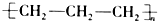 | B. | 丙烷分子的比例模型: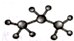 | ||
| C. | 醛基的电子式: | D. | 三硝基甲苯的结构: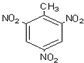 |
分析 A.聚丙烯分子中的结构单元为-CH2-CH2(CH3)-;
B.球棍模型主要体现的是分子的空间结构和成键类型,比例模型主要体现的是组成该分子的原子间的大小关系;
C.醛基中的O原子最外层达到8电子稳定结构;
D.三个硝基取代苯环上的甲基邻位、对位H生成三硝基甲苯.
解答 解:A.聚丙烯为丙烯通过加聚反应生成的,其正确的结构简式为: ,故A错误;
,故A错误;
B. 为丙烷的球棍模型,丙烷的比例模型为:
为丙烷的球棍模型,丙烷的比例模型为: ,故B错误;
,故B错误;
C.醛基中O原子最外层为8个电子,醛基正确的电子式应为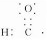 ,故C错误;
,故C错误;
D.甲苯与浓硝酸发生取代反应生成三硝基甲苯,则三硝基甲苯的结构简式为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,涉及电子式、结构简式、比例模型等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
20.将①H+、②Cl-、③NH4+、④K+、⑤S2-、⑥OH-、⑦NO3-分别加入H2O中,基本上不影响水的电离平衡的是( )
| A. | ①③⑤⑦ | B. | ②③⑦ | C. | ①⑥ | D. | ②④⑦ |
7.已知:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol.下列说法不正确的是( )
| A. | 1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3 (g)的能量 | |
| B. | 形成2 mol NH3(g)的化学键释放的总能量大于断裂1 mol N2 (g) 和3 mol H2 (g) 的化学键所吸收的总能量 | |
| C. | 加入催化剂是为了加大反应速率,缩短生产周期,降低生产成本 | |
| D. | 将1 mol N2(g)和3 mol H2(g)充入一密闭容器中充分反应,放出92.2 kJ 的热量 |
17.T℃时,在容积恒定的密闭容器中A气体与B气体反应生成C气体,反应过程中A、B、C浓度的变化如图a所示,若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如图b所示,则下列结论正确的是
( )
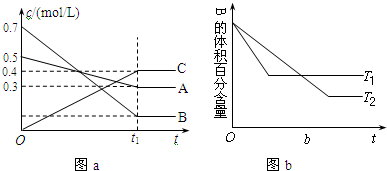
( )

| A. | 其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 | |
| B. | T℃时,若在该容器中由0.4mol/LA、0.4mol/LB和0.2mol/LC反应,达到平衡后,C的浓度仍为0.4mol/L | |
| C. | 在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 | |
| D. | (t1+10)min时,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
4.化学已渗透到人类生活的方方面面,下列说法正确的是( )
| A. | 离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | |
| B. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 | |
| C. | “低碳生活”倡导生活中尽量减少耗能,从而减少CO2排放 | |
| D. | 铝表面有一层致密的氧化物薄膜,故铝制容器可用来腌制咸菜等 |
1.下列粒子的半径最大的是( )
| A. | Na | B. | S | C. | O | D. | Cl |
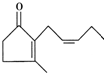 茉莉酮是一种人工合成的香料,其结构简式如图所示:
茉莉酮是一种人工合成的香料,其结构简式如图所示: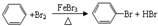 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应. b.
b.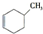 c.
c.
 c.
c.
