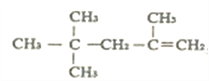
题目内容
【题目】2016年10月17日7点30分,神舟十一号载人飞船发射升空。制造航天飞船的主要材料是铝,工业上制铝时用冰晶石(Na3AlF6)做助熔剂,冰晶石制备流程有如下两种:
方案一:以纯碱和萤石(CaF2)为主要原料
![]()
方案二:以碳酸氢铵和六氟合硅酸为主要原料

(1)方案一中B可作为建筑材料,化合物A 是________,写出由C制备冰晶石的化学方程式____________________________。
(2)方案二中反应1产生的气体是_____________,反应2后滤液中主要成分的用途_________。
(3)方案二中反应2化学方程式________________________。
(4)工业电解制铝的阴极反应式为_________________,以石墨为电极维持电流180千安电解5小时生成铝270千克,则电流效率η(η=实际产量/理论产量)为_______。(法拉第常数F = 96500 C·mol-1)
【答案】 浓硫酸 12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O CO2 用作氮肥 12NH4Cl+Al2(SO4)3+Na2SO4= 2Na3AlF6↓+(NH4)2SO4 Al3++3e-=Al 89.4%
【解析】(1)B是常用建筑材料为硫酸钙,故A是浓硫酸,气体C是HF,反应是HF与Na2CO3、Al(OH)3反应,故方程式为12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O;
(2)从元素守恒看气体是CO2,滤液的中主要成分是(NH4)2SO4,常用作氮肥;
(3)化学方程式为12NH4Cl+Al2(SO4)3+Na2SO4= 2Na3AlF6↓+(NH4)2SO4;
(4)阴极反应式为Al3++3e-=Al,电量Q=180×103A×5h=180×103×5×3600C,电解生成的铝转移电子电量为![]() C,电流效率为η=
C,电流效率为η=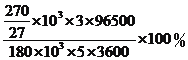 =89.4%。
=89.4%。

【题目】在某温度下,向三个初始体积均为1L的密闭容器中按下表所示投料,发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)△H<0。达到平衡进,下列说法正确的是
2SO3(g)△H<0。达到平衡进,下列说法正确的是
容器编号 | 容器类型 | 起始物质的量/mol | 平衡时SO3的 物质的量/mol | ||
SO2 | O2 | SO3 | |||
Ⅰ | 恒温恒容 | 2 | 1 | 0 | 1.2 |
Ⅱ | 绝热恒容 | 0 | 0 | 2 | a |
Ⅲ | 恒温恒压 | 2 | 1 | 0 | b |
A. 平衡时SO3的物质的量:a>1.2、b>1.2
B. 容器Ⅱ、Ⅲ中平衡常数相同
C. 容器I中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
D. 若起始时向容器Ⅰ中充入1.0molSO2(g)、0.40molO2(g)和1.40molSO3(g),则此时V正<V逆