题目内容
【题目】已知海水中的溴含量约为65mg·L-1,从海水中提取溴的工业流程如图:
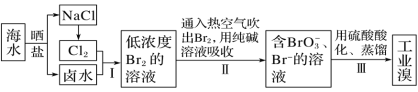
(1)上述步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将其转化成化合态的溴,目的是_____。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的______(填字母)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在方框内填入正确的化学计量数,并将配平后的反应写在答题纸相应位置。_____
![]()
(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为_____。
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有______(填字母)。
A.乙醇 B.四氯化碳 C.裂化汽油 D.苯
【答案】富集(或浓缩)溴元素 C 3,3,1,5,3 Br2+SO2+H2O=2Br-+![]() +4H+ BD
+4H+ BD
【解析】
根据流程,海水晒盐后得到卤水和氯化钠,电解氯化钠溶液可以得到氯气,氯气将卤水中Br-氧化为Br2,得到低浓度的溴水,利用溴的挥发性,使用热空气吹出Br2用纯碱吸收,得到含有![]() 和Br-的混合液,加入硫酸提供酸性环境,发生归中反应得到高浓度的溴水,蒸馏得到工业溴。通过步骤Ⅱ和Ⅲ使较低浓度的溴水变为高浓度溴水起到富集作用,从而降低直接蒸馏提纯的成本,据此分析解答。
和Br-的混合液,加入硫酸提供酸性环境,发生归中反应得到高浓度的溴水,蒸馏得到工业溴。通过步骤Ⅱ和Ⅲ使较低浓度的溴水变为高浓度溴水起到富集作用,从而降低直接蒸馏提纯的成本,据此分析解答。
(1)步骤Ⅰ中已获得游离态的溴浓度很低,如果直接蒸馏,生产成本较高,不利于工业生产,步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是富集溴元素,降低成本,故答案为:富集溴元素;
(2)溴易挥发,步骤Ⅱ通入热空气或水蒸气吹出Br2,就是利用溴的挥发性,故答案为:C;
(3)该反应中Br元素化合价由0价变为-1价、+5价,其最小公倍数是5,再结合原子守恒或电荷守恒得方程式为:3Br2+3![]() =
=![]() +5Br-+3CO2↑,故答案为:3,3,1,5,3;
+5Br-+3CO2↑,故答案为:3,3,1,5,3;
(4)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.溴与二氧化硫水溶液反应生成硫酸和溴化氢,反应的离子方程式为:Br2+SO2+H2O=2Br-+![]() +4H+,故答案为:Br2+SO2+H2O=2Br-+
+4H+,故答案为:Br2+SO2+H2O=2Br-+![]() +4H+;
+4H+;
(5)萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解度、萃取剂和原溶剂不互溶。
A.乙醇易溶于水,所以不能作萃取剂,故A正确;
B.四氯化碳符合萃取剂选取标准,所以能作萃取剂,故B正确;
C.裂化汽油中含有烯烃,可与溴发生加成反应,不能做萃取剂,故C错误;
D.苯符合萃取剂选取标准,所以能作萃取剂,故D正确;
故选BD。

【题目】研究化学反应的能量变化和速率变化是研究化学反应的重要角度。
(1)化学反应中能量变化的主要原因是旧的化学键断裂会_____能量;新的化学键形成会_____能量。(填“放出”或“吸收”)
(2)用铝热法可冶炼铁,其反应为:Fe2O3+2Al![]() 2Fe+Al2O3,属于放热反应,反应物的总能量______(填“>”、“=”或“<”)生成物的总能量。在该反应中,若消耗了1molAl,则理论上可炼制Fe的物质的量为_____mol。
2Fe+Al2O3,属于放热反应,反应物的总能量______(填“>”、“=”或“<”)生成物的总能量。在该反应中,若消耗了1molAl,则理论上可炼制Fe的物质的量为_____mol。
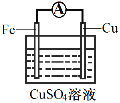
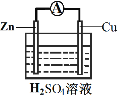
(3)为探究反应过程中的能量变化,某小组同学用如图装置进行实验。
|
|
装置Ⅰ | 装置Ⅱ |
①装置Ⅰ中,Fe与CuSO4溶液反应的离子方程式是_____。
②装置Ⅱ中,正极的电极反应式为______。
③关于装置Ⅱ,下列叙述正确的是______(填字母)。
a.H+在Cu表面被还原,产生气泡
b.电流从Zn片经导线流向Cu片
c.电子从Zn片经导线流向Cu片
d.Zn和Cu的都是电极材料,也都参与电极反应
(4)某兴趣小组将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是_____。
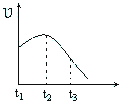
A.从t1→t2的原因是镁与酸的反应是放热反应,体系温度升高
B.从t1→t2的原因水蒸发,致使酸的浓度升高
C.从t2→t3的原因是随着反应的进行镁条的质量下降
D.从t2→t3的原因是随着反应的进行,H+的浓度逐渐下降