题目内容
近来,制备和利用氢气这一清洁能源已有多项成果。
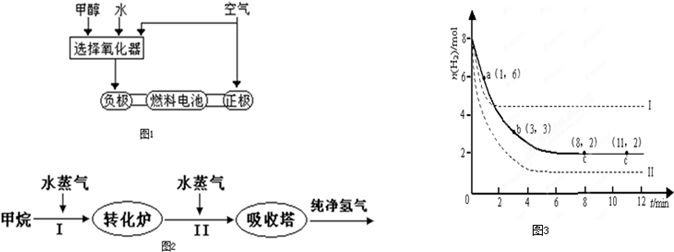
(1)德国克莱斯公司成功研制了车载甲醇(CH3OH)制氢燃料电池工艺,其原理如下图所示,请观察此图回答
(1)德国克莱斯公司成功研制了车载甲醇(CH3OH)制氢燃料电池工艺,其原理如下图所示,请观察此图回答
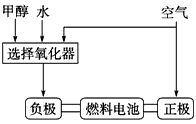
①燃料电池的正极反应式为____________________________。
②甲醇与流程图中任一反应物反应制取氢气的化学方程式________________________。
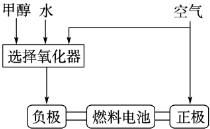
(2)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图
②甲醇与流程图中任一反应物反应制取氢气的化学方程式________________________。
(2)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图
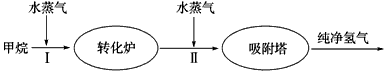
①此流程的第Ⅱ步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
________。
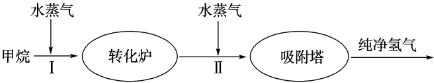
②此流程的第Ⅱ步反应的平衡常数随温度的变化如下表,在830℃、以表中的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有________(填实验编号)。
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=________。
②此流程的第Ⅱ步反应的平衡常数随温度的变化如下表,在830℃、以表中的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有________(填实验编号)。

③若400 ℃时,第Ⅱ步反应生成1 mol氢气的热效应值为33.2(单位为kJ),第Ⅰ步反应的热化学方程式为:
CH4(g)+H2O(g)==3H2(g)+CO(g) ΔH=-103.3 kJ·mol-1 则400 ℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为______________________。
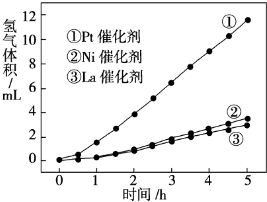
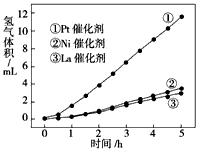
(3)我国科学家研究了常温下利用Pt等催化剂在可见光作用下使水分解制氢气的方法,下图是三种催化剂在光照分解水实验中的效果比较图。能得出如图结果的实验方案是_____________________。
CH4(g)+H2O(g)==3H2(g)+CO(g) ΔH=-103.3 kJ·mol-1 则400 ℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为______________________。
(3)我国科学家研究了常温下利用Pt等催化剂在可见光作用下使水分解制氢气的方法,下图是三种催化剂在光照分解水实验中的效果比较图。能得出如图结果的实验方案是_____________________。
(1)①O2+2H2O+4e-==4OH-;②CH3OH+H2O==2CO2+3H2或2CH3OH+O2==2CO2+4H2或2CH3OH+
H2O==CO2+CO+5H2或4CH3OH+O2===2CO2+2CO+8H2
(2)①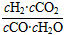 ;②BC;③CH4(g)+2H2O(g)==CO2(g)+4H2(g) ΔH=-136.5 kJ·mol-1
;②BC;③CH4(g)+2H2O(g)==CO2(g)+4H2(g) ΔH=-136.5 kJ·mol-1
(3)控制其他条件不变,每小时测定一次不同催化剂分解水产生氢气的体积,记录数据,作图分析
H2O==CO2+CO+5H2或4CH3OH+O2===2CO2+2CO+8H2
(2)①
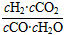 ;②BC;③CH4(g)+2H2O(g)==CO2(g)+4H2(g) ΔH=-136.5 kJ·mol-1
;②BC;③CH4(g)+2H2O(g)==CO2(g)+4H2(g) ΔH=-136.5 kJ·mol-1(3)控制其他条件不变,每小时测定一次不同催化剂分解水产生氢气的体积,记录数据,作图分析

练习册系列答案
相关题目