题目内容
【题目】已知:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4和0.2 mol H2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如下图所示:
CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4和0.2 mol H2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如下图所示:
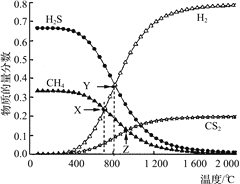
下列说法正确的是( )
A. 该反应的ΔH<0
B. X点CH4的转化率为20%
C. X点与Y点容器内压强比为51∶55
D. 维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1 mol时v(正)<v(逆)
【答案】BD
【解析】A. 由图可知升温平衡右移,所以该反应的ΔH>0,故A错误;B. X点,n(CH4)=n(H2),消耗CH4的物质的量n丿(CH4)=n(H2)/4= n(CH4)/4,所以X点CH4的转化率为20%,故B正确;C. X点容器内气体物质的量为(0.3+2×0.02)mol=0.34mol,Y点,n(H2S)=n(H2),消耗H2S的物质的量n丿(H2S)=n(H2)/2=n(H2S)/2,所以消耗H2S 0.1mol,此时容器内气体物质的量为(0.3+0.1)mol=0.4mol,X点与Y点容器内压强比等于气体物质的量比为17∶20,故C错误; D. 设容器体积为V,Z点,n(CH4)=n(CS2),甲烷转化一半,n(H2)=0.2mol,n(H2S)=0.2mol,平衡常数K=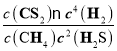 =
=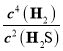 =c2(H2),向容器中再充入CH4、H2S、CS2、H2各0.1 mol时,n(CH4)=n(CS2),n(H2)=0.3mol,n(H2S)=0.3mol,浓度商Q=
=c2(H2),向容器中再充入CH4、H2S、CS2、H2各0.1 mol时,n(CH4)=n(CS2),n(H2)=0.3mol,n(H2S)=0.3mol,浓度商Q= =
=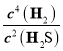 =c2(H2)>K,所以v(正)<v(逆),故D正确。故选BD。
=c2(H2)>K,所以v(正)<v(逆),故D正确。故选BD。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目