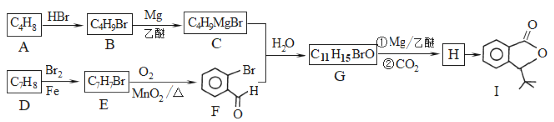
��Ŀ����
����Ŀ��[��ѧ��ѡ��3�����ʽṹ������]
ǰ������ԭ���������������Ԫ��A��B��C��D�У�A��B�ļ۵��Ӳ���δ�ɶԵ��Ӿ�ֻ��1����ƽ��A-��B+�ĵ������Ϊ8����Bλ��ͬһ���ڵ�C��D�����Ǽ۵��Ӳ��е�δ�ɶԵ������ֱ�Ϊ4��2����ԭ���������Ϊ2��
�ش��������⣺
��1��D2+�ļ۲�����Ų�ͼΪ_______��
��2������Ԫ���е�һ������С����________���縺��������________������Ԫ�ط��ţ�
��3��A��B��D����Ԫ����ɵ�һ��������ľ�����ͼ��ʾ��
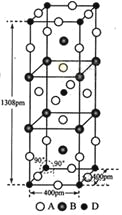
���û�����Ļ�ѧʽΪ_________________��D����λ��Ϊ___________��
����ʽ����þ�����ܶ�_______g��cm-3��
��4��A-��B+��C3+����������ɵĻ�����B3CA6�����л�ѧ����������_____________���û������д���һ���������ӣ������ӵĻ�ѧʽΪ_______________����λ����____________��
���𰸡�![]() K F K2NiF4 6
K F K2NiF4 6 ![]() =3.4 ���Ӽ�����λ�� [FeF6]3- F-
=3.4 ���Ӽ�����λ�� [FeF6]3- F-
��������
��1�����⿼������Ų�ͼ����д��A��B�ļ۵��Ӳ���δ�ɶԵ��Ӿ�ֻ��1�����ӣ�A��Bλ�ڵ�IA�壬���IIIA��Ԫ�ػ�VIIA��Ԫ�أ�A����B���ĵ��������Ϊ8���Ƴ�AΪF��BΪK����Bλ��ͬһ���ڵ�C��D�����Ǽ۵��Ӳ��е�δ�ɶԵ������ֱ�Ϊ4��2����ԭ���������Ϊ2����CΪFe��DΪNi��D2��ΪNi2������۲�����Ų�ͼΪ![]() ��
��
��2����һ������ԽС��˵��Խ����ʧȥ���ӣ���������ǿ����һ��������С����K���縺�����˵���ǽ�������ǿ����F�ĵ縺����ǿ��
��3���ٸ��ݾ����Ľṹ��Fλ�����ϡ������ڲ��������ϣ����F�ĸ���Ϊ16��1/4��4��1/2��2=8��Kλ�����Ϻ��ڲ�������Ϊ8��1/4��2=4��Niλ�ڶ�����ڲ�������Ϊ8��1/8��1=2����˻�ѧʽΪK2NiF4��Ni����λ��Ϊ6��
�ھ���������Ϊ1��(39��4��59��2��19��8)/NA g�����������Ϊ400��400��1308��10-30cm3����˾������ܶ�Ϊ![]() =3.4g/cm3��
=3.4g/cm3��
��4����ɵĻ�ѧʽΪK3FeF6���˻�������������K����FeF63��֮�������Ӽ���Fe��F֮��Ϊ��λ������������[FeF6]3��������ΪF-��

����Ŀ��Ϊ�˼���Ԫ�����ڱ�����150���꣬���Ϲ���2019�궨Ϊ�����ʻ�ѧԪ�����ڱ��������ش��������⣺
(1)Ag��Cu��ͬһ�壬��Ag�����ڱ���_____������s������p������d������ds��������[Ag(NH3)2]+��Ag+�յ�5s�����5p�����sp�ӻ��ɼ�����������ӵĿռ乹����_____��
(2)������Fe��Cu�IJ��ֵ��������ݣ������I2(Cu)����I2(Fe)����Ҫԭ��______��
Ԫ�� | Fe | Cu |
��һ������I1/kJ��mol��1 | 759 | 746 |
�ڶ�������I2/kJ��mol��1 | 1561 | 1958 |
(3)�����軯����ʳ���г��õĿ�������仯ѧʽΪK4[Fe(CN)6]��
��CN-�ĵ���ʽ��______��1mol���������к�������ĿΪ______��
�ڸ�������д��ڵ�������������______������ĸ����
A�������� B�����Ӽ� C�����ۼ� D����λ�� E����� F�����»���
(4)MnO���۵�(1660��)��MnS���۵�(1610��)�ߣ�����Ҫԭ����________��
(5)������̫���ܵ�������л�����±����⻯Ǧ�װ�(CH3NH3PbI3)�뵼����Ϊ������ϣ�CH3NH3PbI3���и��ѿ�(AMX3)�������ṹ���侧����ͼ��ʾ��
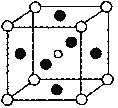
��AMX3�����������������(M)���������±��������(X)�γ���������ṹ����M����_______λ�ã�X����______λ�ã���ѡ��������������������������������������������գ���
��CH3NH3PbI3����ľ�������Ϊa nm���侧���ܶ�Ϊdg��cm-3�����ӵ�������ֵNA�ļ������ʽΪ_________��