题目内容
已知:2SO2(g)+ O2(g) 2SO3(g) △H=-QKJ/mol,在温度一定、容积为2L的密闭容器中分别进行下列三个实验:
2SO3(g) △H=-QKJ/mol,在温度一定、容积为2L的密闭容器中分别进行下列三个实验:
充分作用后,测得实验1反应放出的热量为Q1KJ,实验2没有热量变化,则下列说法中不正确的是( )
A. 实验1放出的热量值为Q1=0.5Q B. 该条件下的平衡常数为:4
C. 实验1中O2的转化率为:50% D. 实验3反应放出热量
 2SO3(g) △H=-QKJ/mol,在温度一定、容积为2L的密闭容器中分别进行下列三个实验:
2SO3(g) △H=-QKJ/mol,在温度一定、容积为2L的密闭容器中分别进行下列三个实验:| 实验编号 | SO2(g) | O2(g) | SO3(g) |
| 1. | 2mol | 1mol | 0mol |
| 2. | 1mol | 0.5mol | 1mol |
| 3. | 1mol | 0.8mol | 1.4mol |
A. 实验1放出的热量值为Q1=0.5Q B. 该条件下的平衡常数为:4
C. 实验1中O2的转化率为:50% D. 实验3反应放出热量
D
实验2没有热量变化,说明恰好是平衡状态。由于三个容器正都是相当于2mol二氧化硫和1mol氧气,因此平衡都是等效的。所以容器1中反应物的转化率是50%,因此放出的热量是0.5Q,选项A、C正确;平衡常数是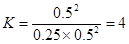 ,选项B正确;实验3中反应是向逆反应方向进行的,因此是吸热放热,选项D不正确,答案选D。
,选项B正确;实验3中反应是向逆反应方向进行的,因此是吸热放热,选项D不正确,答案选D。
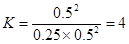 ,选项B正确;实验3中反应是向逆反应方向进行的,因此是吸热放热,选项D不正确,答案选D。
,选项B正确;实验3中反应是向逆反应方向进行的,因此是吸热放热,选项D不正确,答案选D。
练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
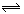 N2O4(g) ΔH﹤0 把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是( )
N2O4(g) ΔH﹤0 把烧瓶置于100℃沸水中,又建立新的平衡状态,前后两平衡比较,不变的是( ) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: 2C(g) ΔH<0。
2C(g) ΔH<0。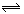 N2O4(g),在体积都为V的A和B两个密闭玻璃容器中,分别注入容积颜色相同的NO2和Br2(气),然后将两个容器体积同时扩大为2V,过一会儿可以看到
N2O4(g),在体积都为V的A和B两个密闭玻璃容器中,分别注入容积颜色相同的NO2和Br2(气),然后将两个容器体积同时扩大为2V,过一会儿可以看到
 C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为 ?nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
?nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答: