题目内容
3.下列有关操作或说法正确的是( )| A. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| B. | 金属汞一旦洒落到实验室地面或桌面时,必须尽可能收集,并深埋处理 | |
| C. | 金属钠着火时用泡沫灭火器灭火 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
分析 A.酸碱中和放出大量的热,且强酸、强碱具有强腐蚀性;
B.汞有毒,具有挥发性,需要用硫单质吸收;
C.金属钠着火生成过氧化钠,与泡沫灭火器喷出的二氧化碳反应;
D.具有吸水性的植物纤维无毒.
解答 解:A.酸碱中和放出大量的热,且强酸、强碱具有强腐蚀性,则浓硫酸溅到皮肤上时立即用抹布擦拭,再水冲洗,最后涂上适量的碳酸氢钠溶液,故A错误;
B.汞挥发的蒸气有毒性,当汞洒落在地面时,由于硫单质能够与汞反应,可以在其洒落的地面上洒上硫粉以便除去汞,故B错误;
C.金属钠着火生成过氧化钠,与泡沫灭火器喷出的二氧化碳反应,反应生成的氧气助燃,不能灭火,应利用沙土铺盖,故C错误;
D.具有吸水性的植物纤维无毒,则可用作食品干燥剂,故D正确.
故选D.
点评 本题考查化学与生活、实验安全,把握物质的性质、实验基本技能、实验安全常识等为解答的关键,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
11.下列有关化学用语表示错误的是( )
| A. | HCN的结构式:H-C≡N | |
| B. | S2-的结构示意图: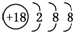 | |
| C. | HClO的电子式: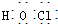 | |
| D. | 质子数为86、中子数为51的铯原子:$\stackrel{137}{86}$Cs |
18.下列离子反应方程式书写正确的是( )
| A. | Fe(OH)3 溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 向 NaAlO2 溶液中通入过量 CO2:AlO2+CO2+2H2O=Al(OH)3↓+HCO3- | |
| C. | 在强碱溶液中次氯酸钠与 Fe(OH)3 反应生成 Na2FeO4 :3ClO-+2Fe(OH)3=2FeO${\;}_{4}^{2-}$+3Cl-+H2O+4H+ | |
| D. | 向硫化钠溶液中滴入氯化铝溶液:2Al3++3S2-=Al2S3↓ |
8.下列叙述中正确的是( )
| A. | 氯化铝溶液中加入过量氨水反应的实质是Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ | |
| B. | 存在于污水中的重金属离子,常用投加明矾等电解质的方法进行处理 | |
| C. | 镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 | |
| D. | 依据铝热反应原理,能发生反应2Al+3MgO$\frac{\underline{\;高温\;}}{\;}$3Mg+Al2O3 |
15.下列说法正确的是( )
| A. | 298K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H>0 | |
| B. | 乙醇、乙二醇、丙三醇互为同系物;H2、D2、T2互为同素异形体 | |
| C. | 用一定浓度的稀盐酸滴定未知浓度的氨水,若选用酚酞作指示剂,会使测定出的氨水物质的量浓度偏低 | |
| D. | 饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,涉及原理相同 |
13.2015年9月28日,美国宇航局宣布发现了火星上存在液态水的证据.下列关于水的叙述正确的是( )
| A. | 水是一种重要的溶剂,能溶解所有的无机物和大多数有机物 | |
| B. | 水是一种重要的化学试剂,在一定条件下可与许多无机物和有机物发生反应 | |
| C. | 在氧化还原反应中,水只能作氧化剂,不能作还原剂 | |
| D. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等,在上述方法中都有化学反应发生 |
 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4次氯酸的强氧化性能杀死水中的病菌.但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4次氯酸的强氧化性能杀死水中的病菌.但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:
 氮可以形成多种化合物,如NO、NH3、N2H4、HCN、NH4NO3等.
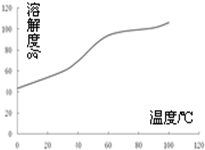
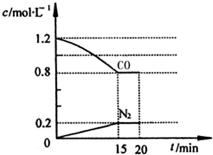
氮可以形成多种化合物,如NO、NH3、N2H4、HCN、NH4NO3等. 2CO2+N2,反应过程中部分物质的浓度变化如图所示:
2CO2+N2,反应过程中部分物质的浓度变化如图所示: