题目内容
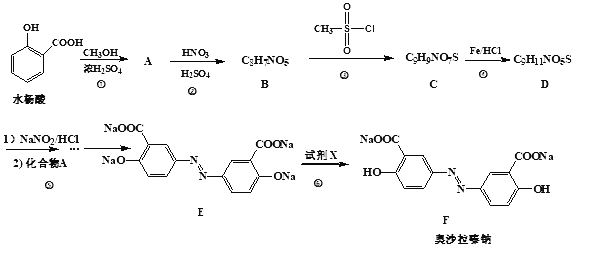
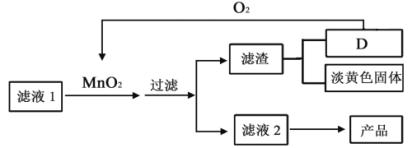
【题目】某研究小组为了探究一种有机盐 X(仅含四种元素)的组成与性质,设计并完成如下实验:

已知: A为两种常见气体的混合物, B、 C 均为常见物质。
(1)X中除含有氢、氧元素外,还含有的元素为:________________(写元素名称)。
(2)写出 X 受热分解的化学方程式:____________________________________________。
(3)设计实验验证“红棕色固体”中金属阳离子______________________________________。
【答案】铁、碳 FeC2O4·2H2O ![]() FeO+2H2O+CO↑+CO2↑ 取少量红棕色固体,加入稀盐酸溶解,滴入几滴硫氰化钾溶液,若溶液变血红色,则含有三价铁
FeO+2H2O+CO↑+CO2↑ 取少量红棕色固体,加入稀盐酸溶解,滴入几滴硫氰化钾溶液,若溶液变血红色,则含有三价铁
【解析】
能使无水硫酸铜变蓝的物质B为水,质量为7.2克,物质的量为0.4mol,红棕色固体为氧化铁,物质的量为16.0g/160g/mol=0.1mol,红褐色沉淀为氢氧化铁,说明白色沉淀2为氢氧化亚铁,则固体C为氧化亚铁0.2mol,二氧化碳和氢氧化钙反应生成白色沉淀为碳酸钙,质量为20克,物质的量为0.2mol,则说明产生的气体A中含有0.2mol二氧化碳。因为A中是混合物,所以应为一氧化碳和二氧化碳。则说明X中含有铁、碳、氧、氢元素。n(CO)=(36g-7.2g-0.2mol×72g/mol-0.2mol×44g/mol)÷28g/mol=0.2mol。
(1)根据以上分析可知,X中含有氢元素和氧元素和铁、碳元素。(2)根据以上分析可知X分解生成0.2mol氧化亚铁质量为14.4克,0.4mol水即7.2克,0.2mol二氧化碳即8.8克,则根据X为36.0克计算一氧化碳的质量为36.0-14.4-7.2-8.8=5.6克,即0.2mol一氧化碳,则方程式为 FeC2O4·2H2O ![]() FeO+2H2O+CO↑+CO2↑。 (3)红棕色固体中的金属阳离子为铁离子,检验铁离子可以利用其与硫氰化钾显红色进行实验,操作为:取少量红棕色固体,加入稀盐酸溶解,滴入几滴硫氰化钾溶液,若溶液变血红色,则含有三价铁。
FeO+2H2O+CO↑+CO2↑。 (3)红棕色固体中的金属阳离子为铁离子,检验铁离子可以利用其与硫氰化钾显红色进行实验,操作为:取少量红棕色固体,加入稀盐酸溶解,滴入几滴硫氰化钾溶液,若溶液变血红色,则含有三价铁。