��Ŀ����
����Ŀ����֪N2��g��+3H2��g��2NH3��g��+Q1��Ӧ���̵������仯������I��˵����ȷ���ǣ� �� 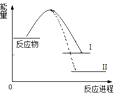
A.1molN��N������3molH��H����֮�ʹ���6molN��H���ܣ����Է�ӦΪ����
B.N2��g��+3H2��g��2NH3��l��+Q2��Ӧ���̵������仯�����ߢ���Q2��Q1
C.ѡ����ʵĴ��������Խ��ͷ�Ӧ�����¶ȣ�Q1ֵҲ��Ӧ����
D.2mol��������������1mol������3mol����������֮�ͣ����Է�Ӧ��Ҫ����
���𰸡�B
���������⣺A����ѧ��Ӧ���ʱ���ھɼ��������յ��������¼������ͷŵ�����֮�1molN��N������3molH��H����֮��С��6molN��H���ܣ����Է�ӦΪ���ȣ���A����
B�������������ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ��Ͳ����������ֵԽ����Ӧ�ų�������Խ����Q2��Q1 �� ��B��ȷ��
C������ֻ�ܸı䷴Ӧ���ʣ�����������ЧӦ�ĸı䣬����ʵĴ������������ܽ��ͷ�Ӧ�����¶ȣ�Q1ֵҲ����ı䣬��C����
D�������������ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����������ڲ������������2mol��������������1mol������3mol����������֮�ͣ���D����
��ѡB��
�����㾫����ͨ��������÷�Ӧ�Ⱥ��ʱ䣬�����ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȼ����Խ����⣮