题目内容
如图所示,通电一段时间后,Cu电极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为100 mL,则通电前A池中原混合溶液Cu2+的浓度为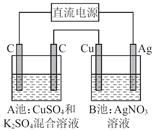
| A.0.05 mol/L | B.0.035 mol/L | C.0.025 mol/L | D.0.020 mol/L |
A
解析“Cu电极增重2.16 g”那么Cu作阴极,则A池中左电极是阴极,右电极是阳极;结合,Ag++e-=Ag,电极增重2.16 g(即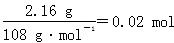 ),转移电子0.02 mol。A池中,阳极反应为4OH--4e-=2H2O+O 2↑,转移0.02 mol电子,即得n(O2)=0.005 mol,累计收集气体224 mL(即
),转移电子0.02 mol。A池中,阳极反应为4OH--4e-=2H2O+O 2↑,转移0.02 mol电子,即得n(O2)=0.005 mol,累计收集气体224 mL(即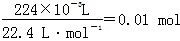 ),那么在阴极还产生0.005 mol H2,阴极反应为2H++2e-=H2↑,转移电子0.01 mol,因此Cu2+放电0.01 mol,Cu2++2e-=Cu,n(Cu2+)=0.005 mol,
),那么在阴极还产生0.005 mol H2,阴极反应为2H++2e-=H2↑,转移电子0.01 mol,因此Cu2+放电0.01 mol,Cu2++2e-=Cu,n(Cu2+)=0.005 mol,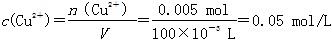 。
。

高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是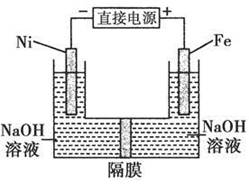
A.铁是阳极,电极反应为Fe-6e-+4H2O= +8H+ +8H+ |
| B.镍电极上的电极反应为2H++2e-=H2↑ |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
某化学学习小组学习电化学后,设计了下面的实验装置图:
下列有关该装置图的说法中正确的是
| A.合上电键后,盐桥中的阳离子向甲池移动 |
| B.合上电键后,丙池为电镀银的电镀池 |
| C.合上电键后一段时间,丙池中溶液的pH增大 |
| D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体 |
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷(C2H6)和氧气,其中某一电极反应式为C2H6+18OH--14e-=2CO32-+12H2O。有关此电池的推断不正确的是
| A.通入氧气的电极为正极 |
| B.参加反应的O2与C2H6的物质的量之比为7∶2 |
| C.放电一段时间后,KOH的物质的量浓度将下降 |
| D.放电一段时间后,正极区附近溶液的pH减小 |
银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,放电时它的正、负两极的电极反应式如下:
Ag2O+H2O+2e-=2Ag+2OH-,Zn+2OH--2e-=Zn(OH)2。
下列判断正确的是( )
| A.锌为负极,氧化银为正极 |
| B.锌为正极,氧化银为负极 |
| C.原电池工作时,负极区溶液pH增大 |
| D.原电池反应的化学方程式为Zn+Ag2O+H2O=Zn(OH)2+2Ag |
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+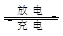 Fe2++Cr3+。下列说法一定正确的是
Fe2++Cr3+。下列说法一定正确的是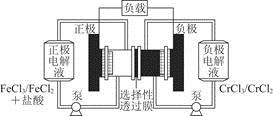
| A.充电时,阴极的电极反应式为Cr3++e-=Cr2+ |
| B.电池放电时,负极的电极反应式为Fe2+-e-=Fe3+ |
| C.电池放电时,Cl-从负极室穿过选择性透过膜移向正极室 |
| D.放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1 |
[双选题]上海人张霞昌在芬兰发明了“纸电池”,这种一面镀锌、一面镀二氧化锰的超薄电池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,纸内的离子“流过”水和氧化锌组成的电解质溶液,电池总反应式为:Zn+2MnO2+H2O=ZnO+2MnOOH。下列说法正确的是( )
| A.该电池的负极材料为锌 |
| B.该电池反应中二氧化锰发生了氧化反应 |
| C.电池的正极反应式为MnO2+H2O+e-=MnOOH+OH- |
| D.当有0.1 mol锌溶解时,流经电解质溶液的电子数为1.204×1023 |
把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将
所得溶液用石墨电极进行电解,阳极生成的物质是( )
| A.H2 | B.Ag | C.Cl2 | D.O2 |
如下图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )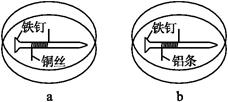
| A.a中铁钉附近呈现红色 | B.b中铁钉上发生还原反应 |
| C.a中铜丝上发生氧化反应 | D.b中铝条附近有气泡产生 |