题目内容
中国尿素合成塔(尿塔)使用寿命仅为欧美国家的1/4。为此北京钢铁研究 院对四川泸天化尿塔腐蚀过程进行研究,得出下列腐蚀机理: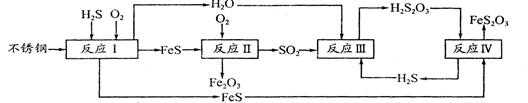
(1)H2S来自合成尿素的天然气。在380 K、体积为2 L的密闭容器中,存在如下反应:H2(g)+S(s) H2S(g) △H=+21.6kJ·mol-1。反应达到平衡时H2、S、H2S的物质的量均为3 mol,则380 K时该反应的化学平衡常数为______;下列对该反应分析正确的是______(填字母序号)。
H2S(g) △H=+21.6kJ·mol-1。反应达到平衡时H2、S、H2S的物质的量均为3 mol,则380 K时该反应的化学平衡常数为______;下列对该反应分析正确的是______(填字母序号)。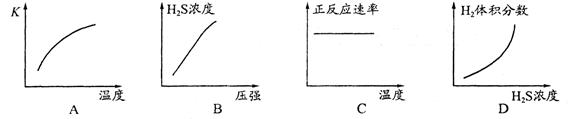
(2)在反应I中发生的化学反应为______。
(3)研究发现反应II是分别以Fe、FeS为电极,以水膜为电解质溶液的电化学腐蚀,其 负
极为______;
已知:Fe(s)+S(s)=FeS(s) △H1=-2.5akJ·mol-1
S(s)+O2(g)=SO2(g) △H2=-5akJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-6akJ·mol-1
则反应II的热化学方程式为_____
(4)已知H2S2O3的K1=2.2×10-1、K2=2.8×10-2。Na2S2O3水溶液呈______性,该溶液中电荷守恒式为_____ ;反应IY的反应类型为______ ;该反应______(填“能”或“不能”) 说明FeS溶解性强于FeS2O3
(5)泸天化尿塔的最终腐蚀产物为______;为了有效防腐,北钢建议泸天化在生产中用 CuSO4溶液“脱硫(H2S)”,其中涉及的离子方程式为
__________________
(1)除去铁钉表面的铁锈;(2)⑤①④②③(3)4Fe+3O2+6H2O=4Fe(OH)3;吸入导管内的品红溶液;(4)铁钉的表面积(温度、催化剂)(5)①溶液的酸性太强,铁容易发生析氢腐蚀;
②6.0<PH≤6.5 ③配置不同浓度的NaCl溶液;
解析试题分析:(1)反应前后气体的体积不变,用平衡时H2、H2S的物质的量代替浓度计算,故该反应的平衡常数k=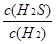 =
=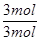 =1;A.该反应正反应是吸热反应,温度升高平衡向正反应移动,平衡常数增大,图象与实际相符合,正确;B.增大压强平衡不移动,但容器体积减小,硫化氢的浓度增大,正确;C.升高温度反应速率加快,图象中正反应速率不变,错误;D.增大硫化氢的浓度,等效为增大压强,平衡不移动,各组分的含量不变,图象与实际不相符,错误;(2)由流程图可知,反应I中铁与硫化氢、氧气反应生成FeS与水,反应方程式为:2Fe+2H2S+O2=2FeS+2H2O;(3)由流程图可知,反应II中FeS与氧气反应生成氧化铁与二氧化硫,FeS发生氧化反应,为负极;已知:①Fe(s)+S(s)═FeS(s)△H1═-2.5akJ/mol;
=1;A.该反应正反应是吸热反应,温度升高平衡向正反应移动,平衡常数增大,图象与实际相符合,正确;B.增大压强平衡不移动,但容器体积减小,硫化氢的浓度增大,正确;C.升高温度反应速率加快,图象中正反应速率不变,错误;D.增大硫化氢的浓度,等效为增大压强,平衡不移动,各组分的含量不变,图象与实际不相符,错误;(2)由流程图可知,反应I中铁与硫化氢、氧气反应生成FeS与水,反应方程式为:2Fe+2H2S+O2=2FeS+2H2O;(3)由流程图可知,反应II中FeS与氧气反应生成氧化铁与二氧化硫,FeS发生氧化反应,为负极;已知:①Fe(s)+S(s)═FeS(s)△H1═-2.5akJ/mol;
②S(s)+O2(g)═SO2(g)△H2═-5akJ/mol9;
③4Fe(s)+3O2(g)═2Fe2O3(s)△H3═-6akJ/mol
根据盖斯定律,③-①×4+②×4得:4FeS(s)+7O2(g)═2Fe2O3(s)+4SO2(g)△H=-16akJ/mol
(4)由电离平衡常数可知,H2S2O3属于弱酸,Na2S2O3为强碱弱酸盐,溶液呈碱性;
阳离子带的电离等于阴离子带的电离,故c(Na+)+c(H+)=2c(S2O32-)+c(HS2O3-)+c(OH-);
反应Ⅳ是H2S2O3与FeS反应生成FeS2O3与H2S,方程式为:H2S2O3+FeS=FeS2O3+H2S↑,符合复分解反应,反应能进行由于生成硫化氢气体,不能说明FeS溶解性更强,(5)由流程图可知,最终腐蚀产物为Fe2O3、FeS2O3;硫化氢与硫酸铜反应生成硫化铜沉淀与硫酸,反应离子方程式为:Cu2++H2S=CuS↓+2H+。
考点:化学平衡常数的含义;金属的电化学腐蚀与防护;难溶电解质的溶解平衡及沉淀转化的本质.

(12分)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:
2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为 。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲v(X)=3.5mol/(L?min);乙v(Y)=2mol/(L?min);丙v(Z)=4.5mol/(L?min);丁v(X)=0.075mol/(L?s)。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号) 。
(3)若向达到(1)的平衡体系中充入氩气,则平衡向 (填"左"或"右"或"不")移动;若向
达到(1)的平衡体系中移走部分混合气体,则平衡向 (填" 左 " 或 " 右 " 或 " 不")移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率⑷与⑴的
平衡中的X的转化率相比较 。
| A.无法确定 | B.⑷一定大于⑴ | C.⑷一定等于⑴ | D.⑷一定小于⑴ |
与(1)的平衡等效,则a、b、c应该满足的关系为 。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为 。
(8分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)。根据题意完成下列问题:
CH3OH(g)。根据题意完成下列问题: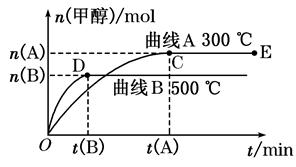
(1)反应达到平衡时,平衡常数表达式K=_________________,升高温度,K值___________(填“增大”、“减小”或“不变”),平衡向 方向移动。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=________________。
(3)在其他条件不变的情况下,将处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是________(选填选项字母)。
| A.氢气的浓度减少 |
| B.正反应速率加快,逆反应速率也加快 |
| C.甲醇的物质的量增加 |
D.重新平衡时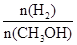 增大 增大 |
在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: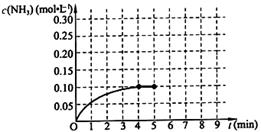
根据图,计算从反应开始到平衡时,平均反应速率v(NH3)= 。
⑵下列描述中能说明上述反应已达平衡的是 。
| A.3v正(H2)=2v逆(NH3) |
| B.容器中气体的平均相对分子量不随时间而变化 |
| C.容器中气体的密度不随时间而变化 |
| D.容器中气体的分子总数不随时间而变化 |
(1)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。某科学实验将6molCO2和8molH2充入2L密闭容器中,测得H2的物质的量随时间变化如右图所示(实线)。图中数据a(1,6)代表的意思是:在l min时H2的物质的量是6mol。
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。某科学实验将6molCO2和8molH2充入2L密闭容器中,测得H2的物质的量随时间变化如右图所示(实线)。图中数据a(1,6)代表的意思是:在l min时H2的物质的量是6mol。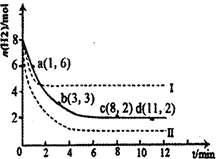
①下列时间段平均反应速率最大的是__________,最小的是______________。
| A.0~1min | B.1~3min | C.3~8min | D.8~11min |
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,等量的CO2和H2O(g)在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图所示。在0~30 h内,CH4的平均生成速率v(Ⅰ)、v(Ⅱ)和v(Ⅲ)从大到小的顺序为 。反应开始后的12小时内,在第___________种催化剂的作用下,收集的CH4最多。

 W (s) + 3H2O (g) 请回答下列问题:
W (s) + 3H2O (g) 请回答下列问题: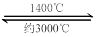 WI4 (g)。下列说法正确的有__________。
WI4 (g)。下列说法正确的有__________。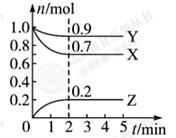
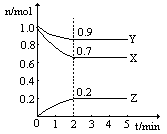
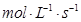 与用物质Y表示的化学反应速率为0.1
与用物质Y表示的化学反应速率为0.1