题目内容
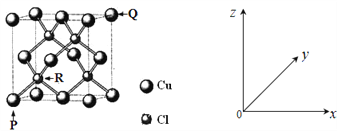
【题目】关于如图结构的说法不正确的是( )
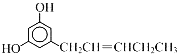
A. 分子中既有![]() 键又有π键
键又有π键
B. 碳原子有sp、sp2、sp3三种杂化方式
C. O—H键的极性强于C-H键的极性
D. 羟基中氧原子采取sp3杂化,VSEPR模型为四面体形
【答案】B
【解析】
A. ![]() 键构成共价单键,
键构成共价单键,![]() 键和π键构成共价苯环、双键或三键,该有机物中含共价单键、苯环和碳碳双键,A项正确;
键和π键构成共价苯环、双键或三键,该有机物中含共价单键、苯环和碳碳双键,A项正确;
B.以4个单键相连的C原子采用sp3杂化方式,苯环和碳碳双键的C原子采用sp2杂化,无sp杂化的C原子,B项错误;
C. 电负性:O>C,则O—H键的极性强于C-H键的极性,C项正确;
D. 羟基中氧原子成键电子对为2,孤电子对为2,则采取sp3杂化,其VSEPR模型为四面体形,D项正确;
答案选B。

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变