题目内容
17.除去下列物质中所含杂质(括号内为杂质),写出除去杂质的化学方程式.(1)Fe2O3[Fe(OH)3]2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
(2)Na2CO3(NaHCO3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
分析 (1)氢氧化铁分解生成氧化铁;
(2)碳酸氢钠加热分解生成碳酸钠,以此来解答.
解答 解:(1)利用加热法可除杂,发生的反应为2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,故答案为:2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O;
(2)利用加热法可除杂,发生的反应为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应及除杂方法为解答关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列说法正确的是( )
| A. | 7.8gNa2O2中所含阴离子的数目是0.2×6.02×1023 | |
| B. | 标准状况下,2.24L18O2中所含中子的数目是6.02×1023 | |
| C. | 1mol甲烷中含共用电子对的数目是4×6.02×1023 | |
| D. | 电解精炼铜时,当阳极溶解6.4g铜,则转移的电子数为6.02×1022个 |
7.下列离子能大量共存的是( )
| A. | 无色酚酞试液呈红色的溶液中:Na+、K+、SO42-、AlO2- | |
| B. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| C. | 含有大量AlO2-的溶液中:Mg2+、Al3+、SO42-、Cl- | |
| D. | 紫色石蕊试液呈红色的溶液中:Ca2+、K+、CO32-、NO3- |
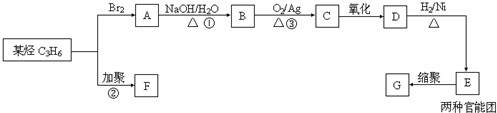
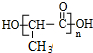 .
.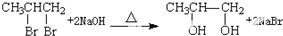 .
. .
. .有机物X的键线式为:
.有机物X的键线式为: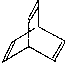


 .
. ,
,
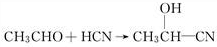 .A→B的反应类型为水解反应或取代反应.
.A→B的反应类型为水解反应或取代反应.