题目内容
7.下列说法正确的是( )| A. | 7.8gNa2O2中所含阴离子的数目是0.2×6.02×1023 | |
| B. | 标准状况下,2.24L18O2中所含中子的数目是6.02×1023 | |
| C. | 1mol甲烷中含共用电子对的数目是4×6.02×1023 | |
| D. | 电解精炼铜时,当阳极溶解6.4g铜,则转移的电子数为6.02×1022个 |
分析 A、求出过氧化钠的物质的量,然后根据1mol过氧化钠中含1mol过氧根构成来分析;
B、求出18O2的物质的量,然后根据1mol18O2中含20mol中子;
C、甲烷中含4mol共用电子对;
D、阳极上放电的除了铜,还有比铜活泼的杂质放电.
解答 解:A、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含1mol过氧根,故0.1mol过氧化钠中含0.1mol阴离子即0.1NA个,故A错误;
B、标况下2.24L18O2的物质的量为0.1mol,而1mol18O2中含20mol中子,故0.1mol中含2mol中子即2NA个,故B错误;
C、甲烷中含4mol共用电子对;,故1mol甲烷中含4mol共用电子对即4NA个,故C正确;
D、阳极上放电的除了铜,还有比铜活泼的杂质放电,故当阳极上溶解6.4g时,转移的电子大于2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
17.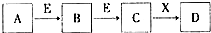 中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
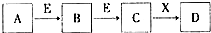 中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| B. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| C. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C | |
| D. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 |
18.宇航员在太空呼吸所需的氧气主要来自太空服中的呼吸面具.下列物质在一定条件下均能产生氧气,其中最适宜用于呼吸面具中供氧的是( )
| A. | HNO3 | B. | H2O2 | C. | KClO3 | D. | Na2O2 |
12.下列关于小苏打水溶液的表述,正确的是( )
| A. | 存在的电离有:HCO${\;}_{3}^{-}$+H2O═H2CO3+OH- | |
| B. | c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$)+c (OH-) | |
| C. | HCO${\;}_{3}^{-}$的电离程度大于HCO${\;}_{3}^{-}$的水解程度 | |
| D. | c(Na+)═c(HCO${\;}_{3}^{-}$)+c (CO${\;}_{3}^{2-}$)+2c(H2CO3) |
19.已知,有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平.A、B、C有如下关系:则下列推断不正确的是( )


| A. | 鉴别A和甲烷可选择使用酸性高锰酸钾溶液 | |
| B. | 乙酸中含有的官能团为羟基 | |
| C. | C的名称为乙酸乙酯 | |
| D. | 过量饮用B会对人体造成伤害 |
16.下列有关SiO2的叙述中错误的是( )
| A. | SiO2是酸性氧化物,它对应的水化物是硅酸(H2SiO3) | |
| B. | 硅酸可由SiO2跟水反应制得 | |
| C. | SiO2可与碱性氧化物或强碱反应 | |
| D. | 光导纤维的主要原料就是SiO2 |