题目内容
【题目】同温同压下,等体积的N2O和CO2两种气体相比较:①质量相等;②所含原子数相等;③所含电子数相等;④所含分子数相等;⑤所含氧原子数相等,上述结论中不正确的是( )
A.③⑤B.②④C.①③D.⑤
【答案】D
【解析】
同温同压下,等体积的气体的物质的量相等,即N2O和CO2的物质的量相等。
![]() 两者的物质的量相等,摩尔质量均为44g/mol,所以质量也相等,
两者的物质的量相等,摩尔质量均为44g/mol,所以质量也相等,![]() 正确;
正确; ![]() 物质的量相等的一氧化二氮
物质的量相等的一氧化二氮![]() 和CO2所含原子数之比=3:3=1:1,则所含原子数相等,
和CO2所含原子数之比=3:3=1:1,则所含原子数相等,![]() 正确;
正确; ![]() 每个分子中电子数均为22,则物质的量相等的一氧化二氮
每个分子中电子数均为22,则物质的量相等的一氧化二氮![]() 和CO2所含电子数相等,
和CO2所含电子数相等,![]() 正确;
正确; ![]() 物质的量相等则所含分子数相等,
物质的量相等则所含分子数相等,![]() 正确;
正确;
⑤等物质的量的两物质,所含氧原子数之比=1:2,所以所含氧原子数不相等,⑤错误;
综上所述,⑤错误,D满足题意。
答案选D。

练习册系列答案
相关题目
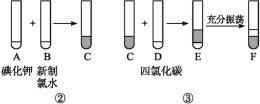
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有还原性 |
B | 向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液,生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
C | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液,溶液变红 | 稀硫酸能氧化Fe2+ |
D | 向AgNO3溶液中滴加过量氨水,得到澄清溶液 | Ag+与NH3·H2O能大量共存 |
A.AB.BC.CD.D