��Ŀ����
��12�֣���1����Ũ�����з���ͭƬ��
�ٿ�ʼ��Ӧ�Ļ�ѧ����ʽΪ___________________________________
����ͭ��ʣ�࣬��Ӧ��Ҫ����ʱ�ķ�Ӧ�����ӷ���ʽ�� ��
�۴���Ӧֹͣ���ټ���������25%��ϡ���ᣬ��ʱͭƬ���������ݲ�������ԭ����
_____________________________________________________��
(2) ��100mL������У�c��HNO3�� = 0��4mol��L-1��c��H2SO4�� = 0��2mol��L-1�������м���2��56gͭ�ۣ��ȣ�����ַ�Ӧ����Һ��Cu2�������ʵ���Ũ��Ϊ ��
��3��14gͭ���Ͻ��������ijŨ�ȵ�������Һ��Ӧ�����ų���������1.12L����״���£��������ͨ��ˮ�У�ǡ��ȫ����ˮ���գ���Ͻ���ͭ�������� ��
�ٿ�ʼ��Ӧ�Ļ�ѧ����ʽΪ___________________________________
����ͭ��ʣ�࣬��Ӧ��Ҫ����ʱ�ķ�Ӧ�����ӷ���ʽ�� ��
�۴���Ӧֹͣ���ټ���������25%��ϡ���ᣬ��ʱͭƬ���������ݲ�������ԭ����
_____________________________________________________��
(2) ��100mL������У�c��HNO3�� = 0��4mol��L-1��c��H2SO4�� = 0��2mol��L-1�������м���2��56gͭ�ۣ��ȣ�����ַ�Ӧ����Һ��Cu2�������ʵ���Ũ��Ϊ ��
��3��14gͭ���Ͻ��������ijŨ�ȵ�������Һ��Ӧ�����ų���������1.12L����״���£��������ͨ��ˮ�У�ǡ��ȫ����ˮ���գ���Ͻ���ͭ�������� ��
(12��)
��1���� Cu + 4HNO3��Ũ��= Cu��NO3��2 + 2NO2�� + 2H2O ��2�֣�
��3Cu + 8H�� + 2NO3�� =3Cu2�� + 2NO�� + 4H2O��2�֣�
���ټ���ϡH2SO4��H����NO3�D������������������2�֣�
��2��0.15mol��L-1 ��3�֣�
��3��3��2g��3�֣�
��1���� Cu + 4HNO3��Ũ��= Cu��NO3��2 + 2NO2�� + 2H2O ��2�֣�
��3Cu + 8H�� + 2NO3�� =3Cu2�� + 2NO�� + 4H2O��2�֣�
���ټ���ϡH2SO4��H����NO3�D������������������2�֣�
��2��0.15mol��L-1 ��3�֣�
��3��3��2g��3�֣�
��1��ͭ�����ᷴӦ����Ũ���йأ�
Cu + 4HNO3��Ũ��= Cu��NO3��2 + 2NO2�� + 2H2O
3Cu + 8HNO3��ϡ��="3" Cu��NO3��2 + 2NO�� + 4H2O
�۴���Ӧֹͣ���ټ���������25%��ϡ�����ṩH������Һ�е�NO3���ɼ�������ͭ
��2��NO3����H����Cu��Ϊ0��04mol�������������ӷ���ʽ��
3Cu + 8H�� + 2NO3�� =3Cu2�� + 2NO�� + 4H2O
0.015mol 0.04mol 0.01mol 0.015mol
��Һ��Cu2�������ʵ���Ũ��Ϊ0.15mol��L-1
(3)��Ͻ���ͭΪx mol����Ϊ y mol
�ɺϽ�������֪��64x+108y=14 �ɵ����غ�ɵã�2x+y=4��11.2/22.4
x=0.05mol y=0.1mol
����ͭΪ3��2g
Cu + 4HNO3��Ũ��= Cu��NO3��2 + 2NO2�� + 2H2O
3Cu + 8HNO3��ϡ��="3" Cu��NO3��2 + 2NO�� + 4H2O
�۴���Ӧֹͣ���ټ���������25%��ϡ�����ṩH������Һ�е�NO3���ɼ�������ͭ
��2��NO3����H����Cu��Ϊ0��04mol�������������ӷ���ʽ��
3Cu + 8H�� + 2NO3�� =3Cu2�� + 2NO�� + 4H2O
0.015mol 0.04mol 0.01mol 0.015mol
��Һ��Cu2�������ʵ���Ũ��Ϊ0.15mol��L-1
(3)��Ͻ���ͭΪx mol����Ϊ y mol
�ɺϽ�������֪��64x+108y=14 �ɵ����غ�ɵã�2x+y=4��11.2/22.4
x=0.05mol y=0.1mol
����ͭΪ3��2g

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
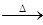 2M+2NO2��+O2��������3.40gMNO3������NO2��O2����ɱ�״��ʱ�������Ϊ672mL���ɴ˿��Լ����M�����ԭ������Ϊ_____________��
2M+2NO2��+O2��������3.40gMNO3������NO2��O2����ɱ�״��ʱ�������Ϊ672mL���ɴ˿��Լ����M�����ԭ������Ϊ_____________��

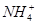 ��H2O ��NH3 ��NH3��H2O ��H+ ��OH-
��H2O ��NH3 ��NH3��H2O ��H+ ��OH- CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O