题目内容
9.下列关于碱金属元素说法正确的是( )| A. | 单质都能在O2中燃烧生成过氧化物 | |
| B. | 从Li到Cs,密度越来越大,熔点越来越低 | |
| C. | 单质都可以保存在煤油中 | |
| D. | 单质都是强还原剂,与水反应都生成强碱 |
分析 A.锂与氧气反应生成氧化锂;
B.碱金属密度从上到下逐渐增大,但是钾反常;熔点从上到下依次减小;
C.锂密度小于煤油;
D.碱金属最外层都只有1个电子,反应中容易失去电子,表现强的还原性,与水反应都生成强碱.
解答 解:A.单质Li能在O2中燃烧只生成氧化物Li2O,不能生成过氧化物,故A错误;
B.从Li到Cs,密度有增大的趋势,在钠和钾出现了反常,故B错误;
C.单质锂密度比煤油的还小,不可以保存在煤油中,该保存在液态石蜡中,故C错误;
D.碱金属单质,易失去电子,表现强的还原性,都能与水反应生成强碱,故D正确;
故选:D.
点评 本题考查了碱金属性质,熟悉同主族元素性质的递变规律是解题关键,注意碱金属密度中钠与钾的反常现象,题目难度不大.

练习册系列答案
相关题目
14.某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据表中的实验现象回答下列问题:
(1)实验1和2中Al所作的电极(正极或负极)不相同(填“相同”或“不相同”).
(2)实验3中负极反应式:Al-3e-=Al3+;总反应的离子方程式:2Al+6H+═2Al3++3H2↑.
(3)实验4中铝作负极,电极反应式:Al-3e-+4OH-═AlO2-+2H2O.
(4)解释实验5中电流计指针偏向铝的原因Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电流由正极流向负极,所以电流计指针偏向铝.
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(1)实验1和2中Al所作的电极(正极或负极)不相同(填“相同”或“不相同”).
(2)实验3中负极反应式:Al-3e-=Al3+;总反应的离子方程式:2Al+6H+═2Al3++3H2↑.
(3)实验4中铝作负极,电极反应式:Al-3e-+4OH-═AlO2-+2H2O.
(4)解释实验5中电流计指针偏向铝的原因Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电流由正极流向负极,所以电流计指针偏向铝.
18.下列说法正确的是( )
| A. | 将AgNO3溶液滴入氨水中制银氨溶液 | |
| B. | 苯酚与苯甲醇(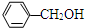 )分子组成相差一个-CH2原子团,因而它们互为同系物 )分子组成相差一个-CH2原子团,因而它们互为同系物 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 苯酚分子中由于羟基对苯环的影响,使苯环上的氢原子容易被取代 |
19.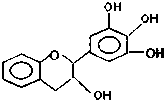 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )| A. | EGC分子中所有的原子一定不共面 | |
| B. | 1mol EGC可以与2molBr2发生取代反应 | |
| C. | EGC可以发生氧化反应和取代反应,1mol该物质可以与6molH2发生加成反应 | |
| D. | 1molEGC与3molNa恰好完全反应 |
 ;
;
 (1)实验室可用如图装置制取乙炔图中A管的作用是调节水面的高度来控制反应的发生和停止,制取乙炔的化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2
(1)实验室可用如图装置制取乙炔图中A管的作用是调节水面的高度来控制反应的发生和停止,制取乙炔的化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2