题目内容
下列关于元素周期表和元素周期律的说法不正确的是
| A.从氟到碘,其氢化物的稳定性逐渐减弱 |
| B.第三周期从钠到铝,最高价氧化物的水化物碱性逐渐减弱 |
| C.因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 |
| D.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 |
C
解析试题分析:A项从氟到碘,非金属性递减,其氢化物的稳定性逐渐减弱,正确;B项第三周期从钠到铝,金属性递减,其最高价氧化物的水化物碱性逐渐减弱,正确;C项虽然铝原子比钠原子失去电子数目多,但铝的金属性比钠弱,其还原性比钠弱,错误;D项氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强,正确。
考点:考查元素周期律。

练习册系列答案
相关题目
据最新报道,放射性同位素钬 Ho可有效地治疗肝癌。该同位素原子的质量数与核电荷数之差为
Ho可有效地治疗肝癌。该同位素原子的质量数与核电荷数之差为
| A.32 | B.67 | C.99 | D.166 |
下列叙述中错误的是 ( )
| A.原子半径Cl>S>O | B.还原性Na>Mg>Al |
| C.稳定性HF>HCl>HBr | D.酸性HClO4>H2SO4>H3PO4 |
今年5月7日某公司丢失铱-192放射源的事件再次敲响核安全的警钟。下列关于铱-192 (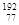 Ir)的说法正确的是
Ir)的说法正确的是
| A.原子序数为77 | B.电子数为115 | C.中子数为192 | D.质量数为77 |
已知下列元素原子的最外层电子排布式,其中不能表示该元素一定为主族元素的是
| A.3s23p3 | B.4s2 | C.4s24p1 | D.3s23p5 |
若aAn+与bB2-两种离子的核外电子层结构相同,则a的数值为( )
| A.b+n+2 | B.b+n-2 | C.b-n-2 | D.b-n+2 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )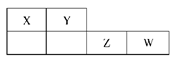
| A.氢化物稳定性:X>Y |
| B.最高价氧化物对应的水化物的酸性:W>Y |
| C.4种元素的单质中,W单质的熔、沸点最高 |
| D.干燥的W单质具有漂白性 |