题目内容
【题目】下图是研究铜与浓硫酸的反应装置:
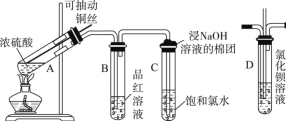
(1)A试管中发生反应的化学方程式为__________
(2)反应一段时间后,可观察到B试管中的现象为___________________
(3)C试管口浸有NaOH溶液的棉团作用是_________________
(4)如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是__________、__________。(要求填一种化合物和一种单质的化学式;如有需要,可加装防倒吸装置)
(5)实验结束后,证明A试管中反应所得产物是否含有铜离子的操作方法是___________
【答案】Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 溶液由红色变成无色 吸收Cl2和SO2防止污染空气 NH3(NO2或ClO2) Cl2(O3或O2或Br2蒸汽) 向上拉铜丝终止反应,冷却后将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色
CuSO4+SO2↑+2H2O 溶液由红色变成无色 吸收Cl2和SO2防止污染空气 NH3(NO2或ClO2) Cl2(O3或O2或Br2蒸汽) 向上拉铜丝终止反应,冷却后将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色
【解析】
根据装置分析可知,装置A中浓硫酸与Cu加热制取SO2,B为检验SO2的漂白性的装置,C为尾气处理装置,若向D装置中通入SO2,要生成白色沉淀,需要加入强氧化剂将BaSO3氧化为BaSO4,据此分析解答。
(1)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)由于反应产生了SO2气体;该气体由漂白性,能使品红溶液褪色。因此反应一段时间后,可观察到B试管中品红溶液由红色变为无色,故答案为:溶液由红色变成无色;
(3)Cl2、SO2气体容易导致大气污染,因为SO2和Cl2气体均能与碱液反应,所以在C试管口用浸有NaOH溶液的棉团来吸收扩散的SO2和Cl2气体,故答案为:吸收Cl2和SO2防止污染空气;
(4)向BaCl2溶液中通入另一种气体,产生白色沉淀,是因为二氧化硫不与氯化钡溶液反应,通入的气体需要满足把二氧化硫转化为盐或把二氧化硫氧化为硫酸,如碱性气体NH3、做氧化剂的气体如Cl2、O2、O3、NO2、Cl2O等,故答案为:NH3;Cl2 ;
(5)实验结束后,若要证明A试管中反应所得产物含有铜离子,操作方法是向上拉铜丝,终止反应,冷却后,将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色,故答案为:向上拉铜丝终止反应,冷却后将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色。