题目内容
A、B、C、D、E原子序数依次增大,且均为短周期元素。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;C和D同周期相邻;D和E同主族相邻;A、C、D三种元素的质子数之和与E(1)A的元素符号是 ,画出E的原子结构示意图 ;(2)写出由A、C、D按4∶2∶3组成的离子化合物的化学式 ,该离子化合物中除具有离子键外还具有 键,写出由A、B、C、D按4∶1∶?2∶1?组成的一种化肥的名称(俗名) ;
(3)B与D组成化合物BD2的电子式为 ,A与C组成的共价化合物C
解析:在短周期中最外层电子数等于其电子层数的元素有H、Be和Al,最外层电子数是次外层电子数的两倍的元素为C,即B为碳元素,所以A应为H元素或者Be元素(可假设为H元素)。设D元素的质子数为m,则C元素的质子数为m-1,E元素的质子数为m+8,所以有m+8=m+(m-1)1,解得m=8,即C为N元素,D为O元素,E为S元素。
![]()
(2)NH4NO3(其他合理也正确) 共价 ?尿素
![]()

练习册系列答案
 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目

 Al(OH)3+3H+
Al(OH)3+3H+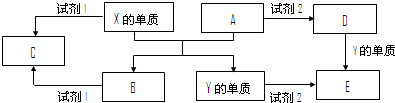
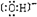
 A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图,B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图,B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
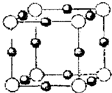 (2012?梧州模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(2012?梧州模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)