题目内容
【题目】如图所示,a中放置附着氧化铜粉末的石棉绒,向a中持续通入气态物质X,可以观察到石棉绒上黑色粉末变成红色固态物质,同时c处的U形管中有无色液体生成(假设X气体全部反应,各处反应均完全)。
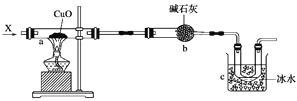
(1)写出a处反应的化学方程式:_______________________________________________。
(2)c处液体主要成分的结构简式为__________________________;检验该物质的操作步骤是_________________________________,其现象为______________________________;有关反应的化学方程式为____________________________________。
【答案】CH3CH2OH+CuO![]() CH3CHO+Cu+H2O CH3CHO取少量c处的液体于试管中,加入新制氢氧化铜悬浊液,加热有砖红色沉淀生成CH3CHO+2Cu(OH)2+NaOH
CH3CHO+Cu+H2O CH3CHO取少量c处的液体于试管中,加入新制氢氧化铜悬浊液,加热有砖红色沉淀生成CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O(或用银镜反应)
CH3COONa+Cu2O↓+3H2O(或用银镜反应)
【解析】
H2、CO和CH3CH2OH蒸气都可以使a中的黑色粉末(氧化铜)变成红色物质(铜),但H2和CO被氧化后的产物分别是H2O和CO2,它们在通过碱石灰后均被吸收,c处的U形管中不会有无色液体生成,因此,X只能是CH3CH2OH蒸气,据此分析可得结论。
(1)在a处反应中乙醇被氧化成乙醛,CuO被还原成Cu,故反应方程式为:CH3CH2OH+CuO![]() CH3CHO+Cu+H2O;(2)c处的U形管中的无色液体为CH3CHO,CH3CHO具有很强的还原性,能被银氨溶液或新制的氢氧化铜悬浊液氧化,利用这两个反应可检验乙醛的存在,故答案为:CH3CHO、 取少量c处的液体于试管中,加入新制氢氧化铜悬浊液,加热、 有砖红色沉淀生成、 CH3CHO+2Cu(OH)2+NaOH
CH3CHO+Cu+H2O;(2)c处的U形管中的无色液体为CH3CHO,CH3CHO具有很强的还原性,能被银氨溶液或新制的氢氧化铜悬浊液氧化,利用这两个反应可检验乙醛的存在,故答案为:CH3CHO、 取少量c处的液体于试管中,加入新制氢氧化铜悬浊液,加热、 有砖红色沉淀生成、 CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O(或用银镜反应)。
CH3COONa+Cu2O↓+3H2O(或用银镜反应)。

 口算能手系列答案
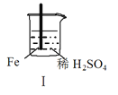
口算能手系列答案【题目】 Fe和Mg与H2SO4反应的实验如下:
实验 |
|
|
|
|
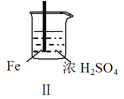
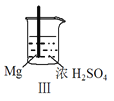
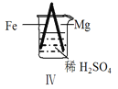
现象 | Fe表面产生大量无色气泡 | Fe表面产生气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是( )
A.I中产生气体的原因是:Fe + 2H+=Fe2++ H2↑
B.取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C.Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D.Ⅳ中现象说明Mg的金属性比Fe强