题目内容
11.“氢能”是未来最理想的新能源.(1)某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤:
①CaBr2+H2O$\frac{\underline{\;750℃\;}}{\;}$CaO+2HBr
②2HBr+Hg$\frac{\underline{\;100℃\;}}{\;}$HgBr2+H2↑
③HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2
④2HgO$\frac{\underline{\;500℃\;}}{\;}$2Hg+O2↑
⑤2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
请你根据“原子经济”的思想完成上述步骤③的化学方程式:HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2.并根据“绿色化学”的思想评估该方法制H2的主要缺点:循环过程需要很高的能量,且用重金属汞,会产生污染.
(2)利用核能把水分解制氢气,是目前正在研究的课题.如图是其中的一种流程,其中用了过量的碘.
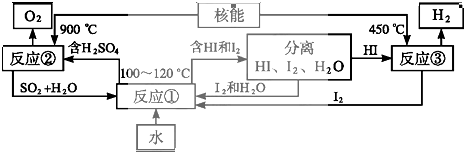
完成下列反应的化学方程式:反应①SO2+I2+2H2O$\frac{\underline{\;100-120℃\;}}{\;}$H2SO4+2HI;反应②2H2SO4═2SO2↑+O2↑+2H2O.此法制取氢气的最大优点是SO2和I2循环使用,避免了污染环境.
分析 (1)根据原子经济分析,反应是原材料分子中的原子全部转变成所需产物,不产生副产物,实现零排放;
(2)根据反应①②写出反应化学方程式,根据制备氢气的过程使用的物质、能量的消耗、环境的污染污染等方面进行分析.
解答 解:(1)理想的原子经济性反应是原材料分子中的原子全部转变成所需产物,不产生副产物,实现零排放.原子利用率是指反应物中的所有原子进入期望产物中的百分比,绿色化学的特征之一是提高原子用率,尽量达到100%,根据原子经济,可知最终反应为:2H2O═2H2↑+O2↑,根据盖斯定律将(①+②+③)×2+④,可知反应③为HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2;该方法中需要750℃,消耗能量高,且有重金属污染,
故答案为:HgBr2+CaO$\frac{\underline{\;250℃\;}}{\;}$HgO+CaBr2;循环过程需要很高的能量,且使用重金属汞,产生污染;
(2)由制备氢气的过程可知,反应①发生的反应是:SO2+I2+2H2O$\frac{\underline{\;100-120℃\;}}{\;}$H2SO4+2HI,反应②是H2SO4分解为了SO2、O2和H2O,故发生的反应为:2H2SO4═2SO2↑+O2↑+2H2O,用该法制取氢气最大的优点是:SO2和I2循环使用,避免了污染环境;
故答为:SO2+I2+2H2O$\frac{\underline{\;100-120℃\;}}{\;}$H2SO4+2HI;2H2SO4═2SO2↑+O2↑+2H2O;SO2和I2循环使用,避免了污染环境.
点评 本题考查热化学方程式的书写、化学方程式的书写等知识,综合性强,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.将X和Y加入密闭容器中,在一定条件下发生反应:X(g)+Y(s)?2Z(g)+W(s).忽略固体所占体积,平衡时Z的体积分数(%)随温度和压强的变化如表所示.
请回答下列问题:
(1)该反应的△S>(填“>”、“<”或“=”,下同)0;△H>0.
(2)表中该反应的化学平衡常数的值最大时对应的温度是1000℃;判断理由是该反应的正反应为吸热反应,升高温度平衡正向移动,平衡常数增大.
(3)在915℃、2.0MPa时X的平衡转化率为60%.
(4)用压强替代浓度得到的平衡常数叫作压强平衡常数(Kp).在810℃、1.0MPa下,Kp=0.634MPa.
(5)能同时提高X的反应速率和转化率的措施是A.
A.升高温度 B.增大压强 C.加催化剂 D分离Z.
| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 85.0 |
(1)该反应的△S>(填“>”、“<”或“=”,下同)0;△H>0.
(2)表中该反应的化学平衡常数的值最大时对应的温度是1000℃;判断理由是该反应的正反应为吸热反应,升高温度平衡正向移动,平衡常数增大.
(3)在915℃、2.0MPa时X的平衡转化率为60%.
(4)用压强替代浓度得到的平衡常数叫作压强平衡常数(Kp).在810℃、1.0MPa下,Kp=0.634MPa.
(5)能同时提高X的反应速率和转化率的措施是A.
A.升高温度 B.增大压强 C.加催化剂 D分离Z.
2.根据甲和乙两个对应的物理量,不能求出物质的量的是( )
| 选项 | 甲 | 乙 |
| A | 物质中的粒子数 | 阿伏加德罗常数 |
| B | 固体体积 | 固体密度 |
| C | 溶液中溶质的物质的量浓度 | 溶液体积 |
| D | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
| A. | A | B. | B | C. | C | D. | D |
19.下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为( )
| A. | 生石灰、漂白粉、氯化铜、碳酸钠 | B. | 胆矾、盐酸、铁、碳酸钙 | ||
| C. | 蒸馏水、氨水、碳酸氢钠、二氧化硫 | D. | 纯盐酸、空气、硫酸、干冰 |
6.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110-120℃时,失去结晶生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+,防止Co2+转化为Co(OH)2沉淀.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+,防止Co2+转化为Co(OH)2沉淀.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
3.下列物质(或主要成分)的化学式错误的是( )
| A. | 重晶石:BaSO4 | B. | 熟石膏:CaSO4•2H2O | ||
| C. | 皓矾:ZnSO4•7H2O | D. | 明矾:KAl(SO4)2•12H2O |
20.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O含有的水分子数为NA | |
| B. | 标准状况下,22.4 L的任何物质的物质的量都约是1 mol | |
| C. | 通常状况下,11.2LCO2的分子数为0.5NA | |
| D. | 常温常压下,0.62g Na2O含有的Na+离子数为0.02 NA |
1.在氢气和氧气的燃烧反应2H2+O2=2H2O中,破坏1mol H2的化学键吸收的能量为A,破坏1mol O2的化学键吸收的能量为B,形成1mol H2O的化学键放出的能量为C,则下列关系正确的( )
| A. | A+B>C | B. | A+B<C | C. | 2A+B<2C | D. | 2A+B>2C |