题目内容
16.在一定体积的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)?xC(g),符合如图所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,P表示压强).在图中Y轴是指( )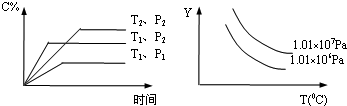
①反应物A的转化率
②平衡混合气中物质B的百分含量
③平衡混合气的密度
④平衡混合气的平均摩尔质量.
| A. | ①③ | B. | ②③ | C. | ③④ | D. | ①④ |
分析 由图可知,相同温度T1时,增大压强(P2>P1),C的百分含量增大,说明增大压强平衡向正反应方向移动,则有a+b>x;
相同压强P2时,升高温度(T1>T2),C的百分含量降低,则说明升高温度平衡向逆反应方向移动,该反应的正反应为放热反应;
由图中Y随温度、压强的变化可知,相同温度下,Y随压强增大而增大;相同压强下,Y随温度增大而减小,结合平衡移动的因素来解答.
解答 解:由图可知,相同温度T1时,增大压强(P2>P1),C的百分含量增大,说明增大压强平衡向正反应方向移动,则有a+b>x;
相同压强P2时,升高温度(T1>T2),C的百分含量降低,则说明升高温度平衡向逆反应方向移动,该反应的正反应为放热反应;
由图中Y随温度、压强的变化可知,相同温度下,Y随压强增大而增大;相同压强下,Y随温度增大而减小,
①增大压强平衡向正反应方向移动,A的转化率增大;升高温度平衡逆向移动,A的转化率减小,则图象中Y可表示A的转化率,故正确;
②增大压强平衡向正反应方向移动,B的百分含量减小,与图象不符,故错误;
③由于反应容器的体积不变,气体的质量不变,则温度、压强变化,平衡混合气的密度不变,故错误;
④升高温度,平衡向逆反应分析移动,则混合气体的物质的量增多,质量不变,则平衡混合气的平均摩尔质量减小,增大压强,平衡向正反应方向移动,气体的总物质的量减小,则平衡混合气的平均摩尔质量增大,则图象中Y可表示A的转化率,故正确;
故选D.
点评 本题考查化学平衡的图象,为高频考点,注意曲线的变化趋势,把握平衡移动的影响因素为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
6.下列叙述正确的是( )
| A. | 二氧化硅是酸性氧化物,不与任何酸反应 | |
| B. | 因为CO2通入水玻璃中可制得硅酸,说明碳酸的酸性比硅酸酸性强 | |
| C. | 水玻璃是一种矿物胶,黏性强,性质稳定,在空气中不易变质 | |
| D. | 石英玻璃是纯净物 |
7.等物质的量的PCl5(g)分别放入起始体积相同的恒压容器A和恒容容器B中,相同温度下反应:PCl5(g)?PCl3(g)+Cl2(g)达到平衡时,两容器中PCl5的分解率相比(用X表示)( )
| A. | XA>XB | B. | XA<XB | C. | XA=XB | D. | 无法确定 |
4.下列各组元素中,已知A、B两种元素的原子序数,其中可组成AB3型离子化合物的是( )
| A. | 6和9 | B. | 13和9 | C. | 11和8 | D. | 12和17 |
11.下列叙述正确的是( )
| A. | 48 g O3气体含有6.02×1023个O3分子 | |
| B. | 常温常压下,4.6g NO2气体含有1.81×1023个NO2分子 | |
| C. | 0.5mol/LCuCl2溶液中含有3.01×1023个Cu2+ | |
| D. | 标准状况下,33.6L 水含有9.03×1023个H2O分子 |
1.原电池发生的反应是可自发进行的氧化还原反应,CO/O2燃料电池以熔融状态的碳酸盐为电解质,下列说法正确的是( )
| A. | 该电池电解质在固态时,电池无法工作 | |
| B. | CO32- 在电池内部向正极移动 | |
| C. | CO在正极通入 | |
| D. | 当有22.4LCO参加反应时电路中有2mol电子发生转移 |
8.下列实验方案不能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 确定苯中是否有酒精 | 向苯和酒精的混合液中加入金属钠 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入适量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 |
| D | 检验制得气体是否为乙烯 | C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
5.下列物质的体积约为22.4L的是( )
| A. | 标准状况下1mol H2O | |
| B. | 20℃、101 kPa时36.5g HCl | |
| C. | 标准状况下80g CuO | |
| D. | 标准状况下0.4 mol H2和0.6mol O2的混合气 |
6.X和Y是短周期元素,二者能形成化合物X2Y3,若Y的原子序数为n,则X的原子序数不可能是( )
| A. | n-8 | B. | n-3 | C. | n-1 | D. | n+5 |