��Ŀ����
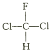
����Ŀ��ijͬѧ̽��Mg��NO2�ķ�Ӧ���ͨ������������֪ʶ�ã�Mg��NO2��Ӧ������MgO��N2���������ʵ�顣
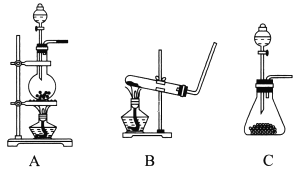
(1)ʵ��������Cu��ŨHNO3�Ʊ�NO2��ѡ�õ�װ����_________________(����ĸ)��������Ӧ�Ļ�ѧ����ʽΪ_________________��
(2)ѡ����ͼ��ʾװ�����Mg��NO2��ʵ�顣
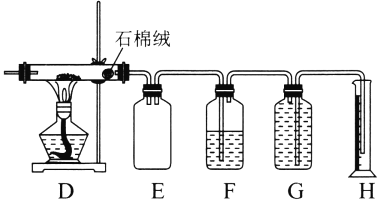
��װ��E������Ϊ_________________��
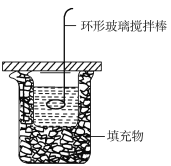
��װ��D�е�������_______________��װ��F��NaOH��Һ������Ϊ_______________��
�۸�װ��________(������������������)ȷ����N2�����ԭ��Ϊ________________��
���𰸡�C Cu+4HNO3(Ũ)=Cu(NO3)2 +2NO2��+2H2O ��ֹ���� ����ɫ��ĩ��ɺ�ɫ��ͨ���������ɫ��dz ��ȥδ��Ӧ�Ķ����������壨���ȥ�����еĶ��������� ���� װ���еĶ�����̼������������Һ���գ�Ӱ��ⶨ���������
��������
(1)����Cu��ŨHNO3�Ʊ�NO2�����ڹ����Һ�巴Ӧ������Ҫ�����Ʊ����壬�ݴ�ѡ��ʹ�õ�װ�ã�
(2)�ٸ��ݶ�������������ˮ�����ܹ���ˮ��Ӧ������𣻢�װ��D��Mg��NO2��Ӧ������MgO��N2���ݴ�����ʵ�������ݹ�������巴Ӧ��������ȫ��Ӧ�����NaOH�����ʷ�����𣻢۴�װ����ԭ��Ϊ�����������к��ж�����̼��������̼�ܹ��������������շ����жϡ�
(1)ʵ��������Cu��ŨHNO3�Ʊ�NO2�����ڹ����Һ�巴Ӧ������Ҫ�����Ʊ����壬Ӧ��ѡ��װ��C����Ӧ�Ļ�ѧ����ʽΪCu+4HNO3(Ũ)=Cu(NO3)2 +2NO2��+2H2O���ʴ�Ϊ��C��Cu+4HNO3(Ũ)=Cu(NO3)2 +2NO2��+2H2O��
(2)�ٶ�������������ˮ�����ܹ���ˮ��Ӧ��������ɵ�����װ��EΪ��ȫƿ�����Է�ֹ�������ʴ�Ϊ����ֹ������
��װ��D��Mg��NO2��Ӧ������MgO��N2�����Կ�������ɫ��ĩ��ɺ�ɫ��ͨ���������ɫ��dz��װ��F��NaOH��Һ���Գ�ȥδ��Ӧ�Ķ����������壬�ʴ�Ϊ������ɫ��ĩ��ɺ�ɫ��ͨ���������ɫ��dz����ȥδ��Ӧ�Ķ�����������(���ȥ�����еĶ�������)��
������װ����ԭ��Ϊ�����������к��ж�����̼��������̼�ܹ��������������գ���ɵ������������ƫ���˸�װ�ò���ȷ����N2������ʴ�Ϊ�����ܣ�װ���еĶ�����̼������������Һ���գ�Ӱ��ⶨ�����������

 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�