题目内容
【题目】某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的数据如下表所示:

实验编号 | 水果种类 | 电极间距离/cm | 电流大小/μA |
① | 西红柿 | 1 | 98.7 |
② | 西红柿 | 2 | 72.5 |
③ | 苹果 | 2 | 27.2 |
(1)该实验的目的是探究水果种类和________对水果电池电流大小的影响。
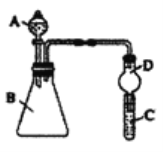
(2)上图所示的装置中,做负极的材料是______(填“锌片”或“铜片”),该装置给将_________转变为电能。
(3)能表明水果种类对电流大小有影响的实验编号是____和_______。
(4)请你再提一个可能影响水果电池电流大小的因素:______________ 。
【答案】电极间距离 锌片 化学能 ② ③ 电极插入水果的深度
【解析】
水果中含有大量的酸性物质,与铜片、锌片可以构成原电池反应,本实验通过改变水果种类和电极之间的间距探究影响水果电池电流大小的因素,据此分析。
(1)根据表格可以分析,水果的种类有2种,电极的间距有2个距离,说明本实验考察的是水果种类对电流大小的影响和电极间距对电流大小的影响,故答案为:电极间距离;
(2)因Zn的活动性比Cu强,故负极材料为锌片;该装置为原电池装置,可以将化学能转化为电能,故答案为:锌片;化学能;
(3)为验证水果种类对电流大小的影响,需要保证电极间距相同,故选择的实验组为②③,答案为②;③;
(4)根据原电池的构成条件,使用同一种水果,保持电极间距不变,改变插入深度,观察电流与深度的关系,故答案为电极插入水果的深度。

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目