题目内容
7.下列各组离子在指定溶液中一定能大量共存的是( )| A. | 使紫色石蕊试纸变红色的溶液:K+、Fe2+、NO3-、Ca2+ | |
| B. | 加入铝粉产生氢气的溶液:SO42-、Cl-、K+、Mg2+ | |
| C. | 含有较多Al3+的溶液:SO42-、Na+、Mg2+、NO3- | |
| D. | 含有较多Fe2+的溶液:Na+、SO42-、ClO-、Cl- |
分析 A.使紫色石蕊试纸变红色的溶液,显酸性,离子之间发生氧化还原反应;
B.加入铝粉产生氢气的溶液,为非氧化性酸或强碱溶液;
C.含有较多Al3+的溶液,显酸性,该组离子之间不反应;
D.离子之间发生氧化还原反应.
解答 解:A.使紫色石蕊试纸变红色的溶液,显酸性,H+、Fe2+、NO3-发生氧化还原反应,不能大量共存,故A错误;
B.加入铝粉产生氢气的溶液,为非氧化性酸或强碱溶液,强碱溶液中不能大量存在Mg2+,故B错误;
C.含有较多Al3+的溶液,显酸性,该组离子之间不反应,可大量共存,故C正确;
D.ClO-、Fe2+发生氧化还原反应,不能大量共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,综合性较强,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.铝电池性能优越,Al-AgO电池主要用于军用水下动力,其工作原理如图所示.下列有关Al-AgO电池的说法错误的是( )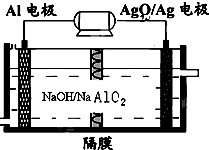

| A. | 正极反应中有Ag生成 | |
| B. | OH-通过隔膜从正极区移向负极区 | |
| C. | 消耗5.4g Al时,电路中转移0.6mol e- | |
| D. | 电池总反应为:2Al+3AgO=Al2O3+3Ag |
18.下列变化过不需另外加人氧化剂或还原剂就能实现的有( )
| A. | Cl-→Cl2 | B. | Fe3+→Fe2+ | C. | KClO3→KCl | D. | KI→I2 |
2.下列有关实验的说法不正确的有( )
| A. | 向橙色的K2Cr2O7溶液中加适量的浓硫酸充分振荡后橙色变深 | |
| B. | 向装有少量Na2S2O3溶液的试管中滴加适量稀硫酸充分振荡后无明显变化 | |
| C. | 向装有淀粉和KI溶液的试管中滴加适量H2SO4充分振荡后溶液变蓝 | |
| D. | 向装有少量H2O2溶液的试管中加适量CuSO4溶液充分振荡后产生大量气泡 |
12.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| B. | 1.0 L 1.0 mol•L-1 的NaAl02水溶液中含有的氧原子数为2 NA? | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 已知C2H4和C3H6混合物的质量为ag,所含原子总数为$\frac{a{N}_{A}}{14}$ |
 ;
;