题目内容
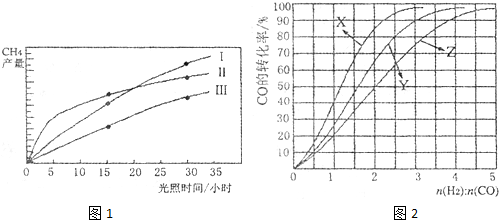
利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图13所示。

(1)在0-30小时内,CH4的平均生成速率VⅠ、VⅡ和VⅢ从大到小的顺序为 ;
反应开始后的12小时内,在第 种催化剂的作用下,收集的CH4最多。
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),该反应的△H=+206 kJ•mol-1
CO(g)+3H2(g),该反应的△H=+206 kJ•mol-1
将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.10mol,求CH4的平衡转化率(计算结果保留两位有效数字)
(3)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g) △H=-802kJ•mol-1
写出由CO2生成CO的热化学方程式
解析:(1)VⅢ>VⅡ> VⅠ;Ⅱ。(2)①略②根据平衡的三步计算可求CH4的平衡转化率为:0.1/0.11=0.91 (3) CO2(g) +3H2O(g) ===2O2(g) +CO(g)+3H2(g) △H=+1008 kJ•mol-1

练习册系列答案
相关题目
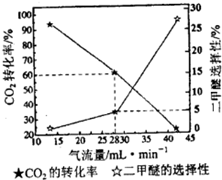
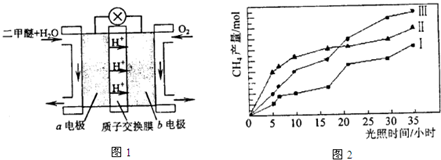

 (2011?广东)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示.
(2011?广东)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示.