题目内容
如果25℃时KW=1×10-14,t℃(t>25)时KW=1×10-12,这说明( )
| A、t℃时水的电离程度较大 |
| B、前者c(H+)较后者大 |
| C、水的电离过程是一个放热过程 |
| D、KW和T(温度)无直接关系 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:水的电离是吸热过程,温度越高,电离程度越大,水的离子积数值越大,氢离子和氢氧根离子浓度越大,但是纯水仍然是中性的.
解答:
解:A、水的电离是吸热过程,温度越高,电离程度越大,t℃时水的电离程度大于常温时的电离程度,故A正确;
B、温度越高,水的离子积数值越大,氢离子和氢氧根离子浓度越大,但始终相等,故B错误;
C、温度越高,电离程度越大,水的电离是吸热过程,故C错误;
D、水的离子积只受温度的影响,和其他因素无关,故D错误;
故选A.
B、温度越高,水的离子积数值越大,氢离子和氢氧根离子浓度越大,但始终相等,故B错误;
C、温度越高,电离程度越大,水的电离是吸热过程,故C错误;
D、水的离子积只受温度的影响,和其他因素无关,故D错误;
故选A.
点评:本题考查学生水的电离以及水的离子积的影响因素知识,注意知识的积累是解题的关键,难度不大.

练习册系列答案
相关题目
2003年10月15日,我国成功发射“神舟五号”载人飞船,飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为:2NH4ClO4═N2↑+Cl2↑+2O2↑+4H2O.下列有关叙述正确的是( )
| A、该反应属于分解反应、氧化还原反应 |
| B、上述反应瞬间能产生大量高温,高温是推动飞船飞行的主要因素 |
| C、铝粉的作用是点燃时氧化放热引发高氯酸铵反应 |
| D、在反应中NH4ClO4仅起到氧化剂作用 |
现已查明非典型肺炎属于急性呼吸道传染病,其病原体是冠状病毒的一种变种.阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤]是抗非典型肺炎(SARS)的指定药物之一,其结构式为:
 .
.
有关阿昔洛韦的结构及性质错误的叙述是( )
 .
.有关阿昔洛韦的结构及性质错误的叙述是( )
| A、分子中所有原子可能在同一平面内 |
| B、该物质在一定条件下可发生消去反应 |
| C、该物质在一定条件下可发生取代反应 |
| D、该物质不属于芳香族化合物 |
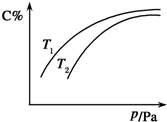 在密闭容器中,对于可逆反应A(?)+3B(?)═2C(g)△H<0,平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
在密闭容器中,对于可逆反应A(?)+3B(?)═2C(g)△H<0,平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )| A、当n(A):n(B):n(c)=1:3:2时,反应达到平衡状态 |
| B、A、B聚集状态均无法确定 |
| C、压强增大时,混合气体的平均相对分子质量增大 |
| D、其他条件不变,升高温度,反应的平衡常数增大 |
氨气溶于水达平衡后,若只改变某一条件,下列说法正确的是( )
A、继续通入氨气,
| ||
| B、NH4Cl水解显酸性,所以向溶液中加入NH4Cl固体,会促进NH3?H2O电离 | ||
| C、向溶液加入HCl气体,则一定有[NH4+]=[Cl-] | ||
| D、实验室中可以通过将浓氨水加入到碱石灰中来制取氨气 |
在100mL溶质的质量分数为30%的稀硫酸中加入100mL蒸馏水所得混合溶液中溶质的质量分数( )
| A、等于15% | B、大于15% |
| C、小于15% | D、无法确定 |
科学家用NaNO3和Na2O在一定条件下化合制得由钠离子和阴离子B构成的晶体NaxNO4,测定阴离子B中的各原子的最外层电子都达到了8电子稳定结构.下列说法错误的是( )
| A、x=3 |
| B、N的化合价为+3 |
C、阴离子B的电子式可能为 |
| D、此反应是非氧化还原反应 |
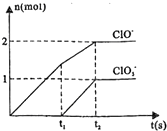 已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.
已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.