题目内容
在恒温恒压条件下,向可变的密闭容器中充入3LA和2LB发生如下反应3A(g)+2B(g)?xC(g)+yD(g),达到平衡时C的体积分数为m%.若维持温度不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%.则x、y的值分别为( )
分析:恒温恒压下,向容积可变的密闭容器中,
状态Ⅰ:3A(g)+2B(g)?xC(g)+yD(g)
起始量 3 2
状态Ⅱ:3A(g)+2B(g)?xC(g)+yD(g)
起始 1.2 0.8 3 0.6
两种状态下到平衡时混合气体中D的体积分数均为W%,
则二者为等效平衡状态,利用极限转化为起始量时,A、B的物质的量之比为3:2,以此来解答.
状态Ⅰ:3A(g)+2B(g)?xC(g)+yD(g)
起始量 3 2
状态Ⅱ:3A(g)+2B(g)?xC(g)+yD(g)
起始 1.2 0.8 3 0.6
两种状态下到平衡时混合气体中D的体积分数均为W%,
则二者为等效平衡状态,利用极限转化为起始量时,A、B的物质的量之比为3:2,以此来解答.
解答:解:由题意可知恒温恒压下,向容积可变的密闭容器中,
状态Ⅰ:3A(g)+2B(g)?xC(g)+yD(g)
起始量 3 2
状态Ⅱ:3A(g)+2B(g)?xC(g)+yD(g)
起始 0.6 0.4 4 0.8
两种状态下到平衡时混合气体中D的体积分数均为W%,
则二者为等效平衡状态,利用极限转化为起始量时,A、B的物质的量之比为3:2,
所以状态Ⅱ:3A(g)+2B(g)?xC(g)+yD(g)
起始 0.6+
0.4+
(0.6+
):(0.4+
)=3:2,
解得x:y=5:1,
显然只有D中x=5、y=1符合,
故选:C.
状态Ⅰ:3A(g)+2B(g)?xC(g)+yD(g)
起始量 3 2
状态Ⅱ:3A(g)+2B(g)?xC(g)+yD(g)
起始 0.6 0.4 4 0.8
两种状态下到平衡时混合气体中D的体积分数均为W%,
则二者为等效平衡状态,利用极限转化为起始量时,A、B的物质的量之比为3:2,
所以状态Ⅱ:3A(g)+2B(g)?xC(g)+yD(g)
起始 0.6+
| 1.2 |
| x |
| 1.6 |
| y |
(0.6+
| 1.2 |
| x |
| 1.6 |
| y |
解得x:y=5:1,
显然只有D中x=5、y=1符合,
故选:C.
点评:本题考查化学平衡的计算及等效平衡,明确两种状态达到平衡时混合气体中D的体积分数均为W%,将第二种状态利用极限转化为起始量成正比即可解答,题目难度中等.

练习册系列答案
相关题目
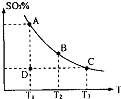 (1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为:2SO2(g)+O2(g)?2SO2(g),反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:
(1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为:2SO2(g)+O2(g)?2SO2(g),反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题: xC(g)+yD(g),达到平衡时C的体积分数为m%.若维持温度不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%.则x、y的值分别为
xC(g)+yD(g),达到平衡时C的体积分数为m%.若维持温度不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%.则x、y的值分别为 xC(g)+yD(g),达到平衡时C的体积分数为m%.若维持温度不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%.则x、y的值分别为
xC(g)+yD(g),达到平衡时C的体积分数为m%.若维持温度不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%.则x、y的值分别为