题目内容
17.100mL6mol•L-1硫酸跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,加入下列物质不能达到实验目的是( )| A. | 硫酸钠(aq) | B. | 硝酸钾(aq) | C. | 醋酸钠(s) | D. | 水 |
分析 过量的锌粉反应,硫酸完全反应,为了减缓反应速率但又不影响生成氢气的总量,可减小氢离子浓度但不改变其物质的量,以此来解答.
解答 解:A.加硫酸钠溶液,不反应,由于体积变大,减小氢离子浓度但不改变其物质的量,反应速率减小,生成氢气的量不变,故A不选;
B.加入硝酸钾,与氢离子、Zn发生氧化还原反应不生成氢气,故B选;
C.加入醋酸钠,生成醋酸,由于醋酸为弱酸,氢离子浓度降低,反应速率减小,但生成氢气的总量不变,故C不选;
D.加入水,浓度降低,反应速率减小,生成氢气的总量不变,故D不选.
故选B.
点评 本题考查影响化学反应速率的因素,为高频考点,注意信息中Zn过量及浓度对反应速率的影响即可解答,注重基础知识的考查,选项B为易错点,题目难度不大.

练习册系列答案
相关题目
7.厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中发生的变化不属于氧化还原反应的是( )
| A. | 用活性炭除去冰箱中的异味 | B. | 燃烧液化石油气为炒菜提供热量 | ||
| C. | 食物长时间放置后变质腐败 | D. | 烧菜用过的铁锅出现红棕色斑迹 |
5.将8g NaOH固体溶于水配成250mL溶液,从中取出50mL,则这50mL NaOH溶液的物质的量浓度为( )
| A. | 0.16 mol•L-1 | B. | 4mol•L-1 | C. | 0.8 mol•L-1 | D. | 8 mol•L-1 |
2.有A、B两个起始容积相等的恒温密闭容器,A保持恒压,B保持恒容.起始时向A、B中均通入2molSO2和1molO2后,在一定条件下反应达到平衡.则下列说法中不正确的是( )
| A. | 达到平衡时,SO2的转化率:A>B | |
| B. | 起始时的反应速率:A=B,反应完成时的平均速率:A>B | |
| C. | 达到平衡后再充入等量氩气,A、B中平衡均不发生移动 | |
| D. | 达到平衡后再向A中充入等量的原反应气体,再次平衡时SO2的质量分数与前次相等 |
9.某烷烃的结构简式为: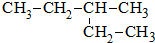 其系统命名正确的是( )
其系统命名正确的是( )
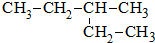 其系统命名正确的是( )
其系统命名正确的是( )| A. | 2-乙基丁烷 | B. | 3-乙基丁烷 | C. | 3-甲基丁烷 | D. | 3-甲基戊烷 |
6.下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆生的观点的是( )
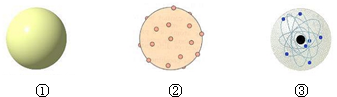

| A. | ①②③ | B. | ③①② | C. | ③②① | D. | ②①③ |
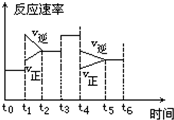 在一密闭体系中发生下列反应:N2+3H2?2NH3 △H<0,如图是某一时间段中反应速率与反应进程的曲线关系图:
在一密闭体系中发生下列反应:N2+3H2?2NH3 △H<0,如图是某一时间段中反应速率与反应进程的曲线关系图: