题目内容
【题目】某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:

(1)写出用稀硫酸溶解碳酸锰反应的离子方程式______________________________。
(2)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.3 |
沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 | 10.8 |
①流程中先加双氧水的目的是__________________________________________。
②加氨水调节溶液的pH等于6,则滤渣的成分是__________________,滤液中含有的阳离子有H+ 和___________________。
(3)在浸出液里锰元素只以Mn2+ 的形式存在,且滤渣中也无MnO2,请解释原因_________。
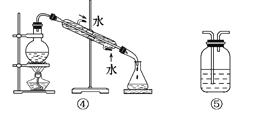
(4)阴离子膜法电解装置如右图所示,电解装置中箭头表示溶液中阴离子移动的方向,则A电极是______极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为__________________________。

(5)该工艺之所以采用阴离子交换膜,是为了防止Mn2+ 进入阳极区发生副反应生成MnO2造成资浪费,写出该副反应的电极反应式________________________________。
【答案】 MnCO3+2H+=Mn2++CO2↑+H2O 将Fe2+氧化为Fe3+ Al(OH)3、Fe(OH)3 Mn2+、Mg2+、NH4+ MnO2在酸性条件下被二价铁还原为Mn2+ 负极 4OH--4e-=O2↑+2H2O或2H2O4e-=O2↑+4H+ Mn2+-2e-+2H20=MnO2+4H+
【解析】(1)用稀硫酸溶解碳酸锰反应的离子方程式为MnCO3+2H+=Mn2++CO2↑+H2O。
(2)①流程中先加双氧水的目的是将Fe2+氧化为Fe3+。
②加氨水调节溶液的pH等于6,由表中数据可知,pH=6时,Fe3+和Al3+可以完全沉淀,其他离子不会沉淀,所以滤渣的成分是Al(OH)3、Fe(OH)3,滤液中含有的阳离子有H+ 和Mn2+、Mg2+、NH4+。
(3)在浸出液里锰元素只以Mn2+ 的形式存在,且滤渣中也无MnO2,因为MnO2在酸性条件下被二价铁还原为Mn2+。
(4)由图可知,溶液中阴离子由左向右移动,则与B相连的电极为阳极,B电极为正极,所以A电极是负极。实际生产中,阳极以稀硫酸为电解液,阳极上OH-放电生成氧气,电极反应式为4OH--4e-=O2↑+2H2O或2H2O4e-=O2↑+4H+。
(5)该工艺之所以采用阴离子交换膜,是为了防止Mn2+ 进入阳极区发生副反应生成MnO2造成资浪费,该副反应的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+。

【题目】某实验科研小组研制了一种从废旧的含镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等)回收镍的新工艺。工艺流程如下图:
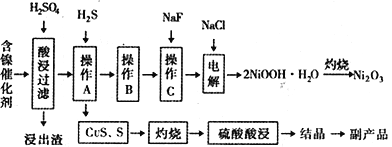
回答下列问题:
(1)浸出渣主要成分为CaSO4↓·2H2O和_______________两种物质。
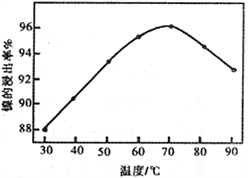
(2)右图表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是_____________________________。
(3)工艺流程中的“副产品”为________(填化学式)。
(4)已知有关氢氧化物开始沉淀和沉淀完全的pH 如下表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.7 | 9.7 | 9.2 |
操作B是为了除去滤液中的铁元素,某同学设计了如下实验方案:向操作A所得的滤液中加入NaOH溶液,调节溶液pH为3.7~7.7,静置,过滤。请对该实验方案是否正确进行判断并做出评价: ___________________________________(若原方案正确,请说明理由;若原方案错误,请加以改正)。
(5)操作C是为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3mol·L-1,则溶液中![]() =________________。(常温时,Ksp(CaF2)=2.7×10-11)
=________________。(常温时,Ksp(CaF2)=2.7×10-11)
(6)电解产生2NiOOH·H2O的原理分两步:
①碱性条件下Cl-在阳极被氧化为ClO-;生产1mol ClO-,消耗OH-______________mol。
②Ni2+被ClO-氧化产生2NiOOH·H2O沉淀。则该步反应的离子方程式为_________________________。