题目内容
15.下列反应的离子方程式正确的是( )| A. | 过氧化钠和水反应:2Na2O2+2 H2O═4Na++4OH-+O2↑ | |
| B. | 氧化铝溶于氢氧化钠溶液:Al2O3+2 OH-═2AlO${\;}_{2}^{-}$+H2↑ | |
| C. | 用小苏打治疗胃酸过多:CO32-+H+═CO2↑+H2O | |
| D. | 二氧化碳通入足量氢氧化钠溶液:CO2+OH-═CO${\;}_{3}^{-}$ |
分析 A.过氧化钠和水反应生成氢氧化钠和氧气;
B.原子个数不守恒;
C.小苏打为碳酸氢钠,碳酸氢根离子不能拆;
D.原子个数不守恒,不符合反应客观事实.
解答 解:A.过氧化钠和水反应生成氢氧化钠和氧气,离子方程式:2Na2O2+2 H2O═4Na++4OH-+O2↑,故A正确;
B.氧化铝溶于氢氧化钠溶液,离子方程式:Al2O3+2OH-═2AlO2-+H2O,故B错误;
C.用小苏打治疗胃酸过多,离子方程式:HCO3-+H+═CO2↑+H2O,故C错误;
D.二氧化碳通入足量氢氧化钠溶液,离子方程式:CO2+2OH-═CO32-+H2O,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应必须遵循客观事实,遵循原子个数、电荷数守恒规律,题目难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
5.在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是( )
| A. | n(Cl2):n(Fe)=5:4 5Cl2+4Fe $\frac{\underline{\;点燃\;}}{\;}$2FeCl2+2FeCl3 | |
| B. | n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2═Fe3++Br2+2Cl- | |
| C. | n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| D. | n(Fe):n[HNO3(稀)]=1:3 4Fe+12H++3NO3-═3Fe2++Fe3++3NO↑+6H2O |
6.在一密闭容器中,反应m A(g)+n B(g)?3C(g)达到平衡时,测得c(A)=0.5mol/L.在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)=0.2mol/L.下列判断中正确的是( )
| A. | A的质量分数增加 | B. | 平衡不移动 | ||
| C. | 化学计量数:m+n=3 | D. | 物质C的体积分数增加 |
3.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 32gO2中含有的分子数为NA | |
| B. | 标准状况下,22.4L H2O中含有的分子数为NA | |
| C. | 1mol Mg与足量O2反应转移的电子数为NA | |
| D. | 1L 1mol•L-1 CaCl2溶液中含有的氯离子数为NA. |
10.雷雨天闪电时空气中有臭氧(O3)生成,下列说法中正确的是( )
| A. | O2和O3互为同素异形体 | |
| B. | O3是由3个氧原子构成的化合物 | |
| C. | O2和O3相互转化属于化学变化 | |
| D. | 等质量的O2和O3含有的氧原子数相同 |
7.对一些具有危险的化学物质,若要在其包装上贴危险化学品标记,下列标签贴错的是( )
| A. | 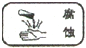 浓硫酸 | B. |  汽油 | C. |  KClO3 | D. |  乙醇 |
5.下列过程放出热量的是( )
| A. | CO燃烧 | B. | 干冰气化 | ||
| C. | 碳酸钙分解 | D. | 氢氧化钡晶体和氯化铵混合 |