题目内容
(16分)
用CaSO4代替O2与燃料CO反应,既可以提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g) 1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
②CaSO4(s)+CO(g) CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
③CO(g) 1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
(1)反应2 CaSO4(s)+7CO(g) CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
(2)反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见图18.结合各反应的△H,归纳lgK~T曲线变化规律:

a)
b)
(3)向盛有CaSO4的真空恒容容器中充入CO,反应①于900 ºC达到平衡,c平衡(CO)=8.0×10-5mol·L-1,计算CO的转化率(忽略副反应,结果保留2位有效数字)。
(4)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入 。
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生成CaSO4,该反应的化学方程式为 ;在一定条件下CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为 。
用CaSO4代替O2与燃料CO反应,既可以提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g)
 1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol②CaSO4(s)+CO(g)
 CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol③CO(g)
 1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol(1)反应2 CaSO4(s)+7CO(g)
 CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。(2)反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见图18.结合各反应的△H,归纳lgK~T曲线变化规律:

a)
b)
(3)向盛有CaSO4的真空恒容容器中充入CO,反应①于900 ºC达到平衡,c平衡(CO)=8.0×10-5mol·L-1,计算CO的转化率(忽略副反应,结果保留2位有效数字)。
(4)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入 。
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生成CaSO4,该反应的化学方程式为 ;在一定条件下CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为 。
(1)4△H1+△H2+2△H3;
(2)a)、放热反应的lgK随温度升高而下降; b)、放出或吸收热量越大的反应,其lgK受温度影响越大;
(3)99%
(4)CO2
(5)CaS+2O2 CaSO4,
CaSO4,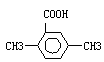
(2)a)、放热反应的lgK随温度升高而下降; b)、放出或吸收热量越大的反应,其lgK受温度影响越大;
(3)99%
(4)CO2
(5)CaS+2O2
 CaSO4,
CaSO4,
试题分析:(1)根据盖斯定律可得2 CaSO4(s)+7CO(g)
 CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H=①×4+②+③×2=4△H1+△H2+2△H3;
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H=①×4+②+③×2=4△H1+△H2+2△H3;(2)由图像及反应的△H可知,a)、反应①③是放热反应,随温度升高,lgK降低;反应②是吸热反应,随温度升高,lgK增大;b)、从图像上看出反应②、③的曲线较陡,说明放出或吸收热量越大的反应,其lgK受温度影响越大;
(3)由图可知,反应①于900 ºC的lgK=2,则K=100, c平衡(CO)=8.0×10-5mol·L-1,平衡时c平衡(CO2)=100×8.0×10-5mol·L-1=8.0×10-3mol·L-1,根据反应1/4CaSO4(s)+CO(g)
 1/4CaS(s)+CO2(g)可知,消耗CO的浓度是8.0×10-3mol·L-1,则开始时c(CO)=8.0×10-5mol·L-1+8.0×10-3mol·L-1=8.08×10-3mol·L-1,所以CO的转化率为8.0×10-3mol·L-1/8.08×10-3mol·L-1×100%=99%,;
1/4CaS(s)+CO2(g)可知,消耗CO的浓度是8.0×10-3mol·L-1,则开始时c(CO)=8.0×10-5mol·L-1+8.0×10-3mol·L-1=8.08×10-3mol·L-1,所以CO的转化率为8.0×10-3mol·L-1/8.08×10-3mol·L-1×100%=99%,;(4)根据方程式可知,二氧化碳中含有气体杂质SO2,可在CO中加入适量的CO2,抑制二氧化硫的产生;
(5)CaS转化为CaSO4,从元素守恒的角度分析,CaS与氧气发生化合反应,原子的利用率100%,生成CaSO4,化学方程式为CaS+2O2
 CaSO4,CO2与对二甲苯发生反应,所得产物中含有羧基,因为苯环的氢原子只有1种,所以产物的结构简式只有1种为
CaSO4,CO2与对二甲苯发生反应,所得产物中含有羧基,因为苯环的氢原子只有1种,所以产物的结构简式只有1种为 。
。
练习册系列答案
相关题目
 时:
时:


 Cl2(g)+CO(g) △H=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下同所示(第10min到14min的COCl2浓度变化曲线未示出):
Cl2(g)+CO(g) △H=+108kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下同所示(第10min到14min的COCl2浓度变化曲线未示出):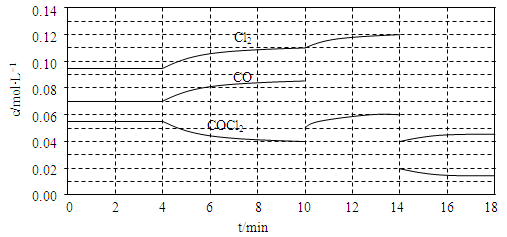
 HOI(aq) △H2
HOI(aq) △H2


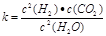 它所对应的化学反应为:__ ___
它所对应的化学反应为:__ ___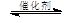 CH3OCH3(g)+ 3H2O(g)
CH3OCH3(g)+ 3H2O(g)