题目内容
【题目】I.人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为_________。电池工作一段时间后需要充电,充电过程中电池液中H2SO4的浓度_____(填“增大”、“减小”或“不变”)。
⑵某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成原电池,则负极发生的电极反应为___________;当反应进行到一段时间后取出电极材料,测得某一电极增重了 5.4g,则该原电池反应共转移了的电子数目是________________________。
⑶燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
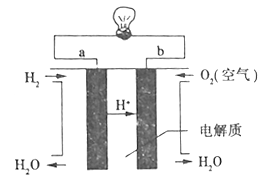
①该电池的正极反应式_________________。
②若该电池的效率80%,当外电路通过0.2mo1电子时,消耗O2的体积____L(标准状况)
II.用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应4HC1+O2 ![]() 2Cl2+2H2O,可实现氯的循环利用。己知上述反应中,4mol HC1被氧化,放出约116kJ的热量。
2Cl2+2H2O,可实现氯的循环利用。己知上述反应中,4mol HC1被氧化,放出约116kJ的热量。
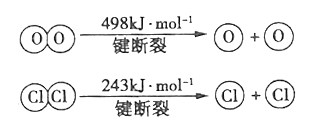
计算断开1 mol H-O键与断开1 mol H-C1键断所吸收能量相差约为______kJ。
【答案】 PbO2+4H++SO42-+2e-=PbSO4+2H2O 增大 Cu-2e=Cu2+ 0.05NA O2+4e+4H+=2H2O 1.4 32
【解析】I.(1)放电时,负极电解反应:Pb-2e-+SO42-=PbSO4 ,正极电极反应:PbO2+2e-+4H++2SO42-=PbSO4+2H2O,根据电池反应式知,充电时硫酸是生成物,所以充电过程中电池液中H2SO4的浓度增大;
⑵由反应“2Ag++Cu═Cu2++2Ag”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,反应式为Cu-2e-=Cu2+;当银电极质量增加5.4g,则n(Ag)=![]() =0.05mol,根据电极反应Ag++e-=Ag,可知导线中通过的电子的物质的量为0.05mol;
=0.05mol,根据电极反应Ag++e-=Ag,可知导线中通过的电子的物质的量为0.05mol;
⑶①氢氧燃料电池,通氧气的极为正极,发生还原反应,该电池的正极反应式O2+4e+4H+=2H2O;
②设参加反应的氧气为VL(标准状况),则![]() ×80%×4mol=0.2mol,解得V=1.4;
×80%×4mol=0.2mol,解得V=1.4;
II.E(H-O)、E(HCl)分别表示H-O键能、H-Cl键能,反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+4×E(H-O)]=-115.6kJ/mol,整理得,4E(H-Cl)-4E(H-O)=-127.6kJ/mol,即E(H-O)-E(HCl)=31.9kJ/mol,
故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ/mol×1mol=31.9kJ≈32kJ。
。