题目内容
【题目】一种白色固体可能由![]() 离子中的若干种组成, 陶宝同学设计实验检验其组成,记录如下:
离子中的若干种组成, 陶宝同学设计实验检验其组成,记录如下:
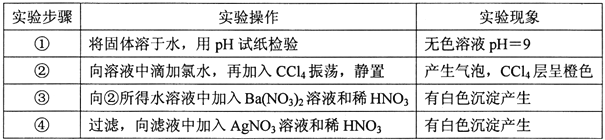
下列关于固体组成的结论错误的是
A. 肯定含有![]() 和
和![]() B. 至少含有
B. 至少含有![]() 中的一种离子
中的一种离子
C. 肯定不含Ba2+,一定含有Cl- D. 无需焰色反应即可断定溶液中含有Na+
【答案】C
【解析】①将固体溶于水,用pH试纸检验,溶液pH=9,该溶液为弱碱性,则可能存在HCO3-、SO32-;②向溶液中滴加氯水,再加入CCl4振荡,静置,产生气泡,CCl4层呈橙色,橙色的为溴单质,则溶液中存在溴离子;气体只能为二氧化碳,则原溶液中存在碳酸氢根离子;③向②所得水溶液中加入Ba(NO3)2溶液和稀HNO3,有白色沉淀产生,该白色沉淀为硫酸钡,原溶液中至少存在SO32-、SO42-中的原则离子,根据离子共存,则一定存在钡离子;④操作步骤中的现象证明含氯离子,但由于②加入了氯离子,所以原溶液是否含氯离子不能确定;最后根据电荷守恒确定原溶液中一定存在钠离子。
A.根据以上分析可知,原溶液中一定存在HCO3-和Br-,故A正确;B.根据③可知原溶液中至少含有SO32-、SO42-中的一种离子,故B正确;C.根据以上分析可知,原溶液中一定不存在钡离子,由于②加入了氯离子,无法确定原溶液中是否存在氯离子,故C错误;D.由于不存在钡离子,根据溶液电中性可知,溶液中一定存在唯一的阳离子钠离子,故D正确;故选C。

练习册系列答案
相关题目
【题目】魔术师将半杯“白酒”倒入半杯“黄酒”中变成了一杯“红酒”,“白酒”和“黄酒”的成分可能是
“白酒” | “黄酒” | |
A | KSCN溶液 | FeCl3溶液 |
B | KOH溶液 | 溴水 |
C | KOH溶液 | 酚酞溶液 |
D | 淀粉溶液 | 碘水 |
A. A B. B C. C D. D